ЦИНК
Цинк (Zn)-тяжелый легкоплавкий металл синевато-белого цвета. Содержание цинка в земной коре 0,005 %. (по массе).
Известно 66 минералов цинка, находящихся в полиметаллических рудах содержащих свинец, медь и железо. Важнейшие из этих минералов цинкит (красная цинковая руда) ZnO, сфалерит (или цинковая обманка) ZnS, виллемит Zn2SiO4, каламин H2Zn2SiO4, смит-сонит ZnCO3, франклинит ZnFe2O4(Fe, Zn, Mn)O(Fe, Mn2O3).
В настоящее время половину производимого в мире цинка получают гидрометаллургическим способом, а половину — пирометаллургическим. Независимо от способа получения, производство цинка начинается с обогащения цинковых руд, так как они содержат небольшие количества цинка (обычно 1-3 %). При селективной флотации получают цинковые концентраты с 48-58 % Zn, 1-2 % Pb, <2 % Cu, 5-10 % Fe и около 30 % S и одновременно пиритные, медные и свинцовые концентраты.
Первая стадия переработки концентратов - обжиг. На всех современных заводах обжиг ведут в кипящем слое или во взвешенном состоянии. В результате получают газы, содержащие 4-6 % SO2, которые поступают на производство серной кислоты.
При пирометаллургическом производстве обжиг совмещают с агло-мерацией, добиваясь, чтобы шихта для последующей дистилляции была кусковой и газопроницаемой. Дистилляцию ведут в ретортах нагревом до 1250-1300 °С смеси обожженного концентрата с коксом. Цинк при этом восстанавливается и испаряется. Пары цинка в смеси с оксидом углерода направляются в конденсатор, в котором при температуре 450-500 °С образуется жидкий цинк.
Цинк полученный дистилляционным способом, содержит от 1 до 3 % примесей, и его подвергают рафинированию сначала ликвацией (от свинца и железа), затем ректификацией (от свинца, кадмия, меди, мышьяка и других примесей). После ректификации металл содержит 99 995 % Zn.
Предварительно очищенный и подвергнутый 26-кратной зонной плавке в токе азота металл содержит 99,999995 % Zn.
В соответствии с ГОСТ 3640—79 цинк поставляют в виде чушек и блоков. Химический состав-см. табл. с. 123. Цинк марки ЦВОО изготовляют в виде чушек массой 5 и 10 кг, цинк марок ЦВО, ЩН, ЦВ, ЦОА, ЦО, Ц1, Ц2, ЦЗ —в виде чушек массой 19—25 кг или в виде блоков массой до 1 т.
Кроме компактного цинка, выпускается цинковый порошок, который изготовляется ректификацией или распылением жидкого металла. Его используют в химической или металлургической промышленности, а также для производства химических источников тока. Маркируются порошки так же, как и компактный цинк, но впереди ставится буква «П», например ПЦВ, ПЦО и т. д. Порошок упаковывают в герметичные металлические барабаны; масса нетто порошка в барабане 30, 40, 50 кг, Хранить порошок следует в сухих закрытых помещениях.
Технологические свойства цинка
Температура литья цинка 430—450 °С. Линейная усадка 1,57%. Жидкотекучесть (длина спирали) 110 см.
При обычной температуре цинк хрупок и плохо поддается обработке давлением, но при 100—150 °С становится пластичным и из него можно получать тонкие листы и проволоку. При повышении температуры пластичность цинка падает: при 200—250 °С он становится очень хрупким и его можно истолочь в порошок.
Примеси свинца, висмута, сурьмы и мышьяка отрицательно влияют на технологические свойства цинка. При горячей обработке давлением цинк, содержащий даже менее 0,05 % Sn, легко разрушается вследствие выделения эвтектики.
Железо задерживает рекристаллизацию цинка и способствует наклепу. При содержании железа >0,2 % в цинке образуется хрупкая металлическая фаза FeZn7; при 0,2 % Fe хрупкость настолько возрастает, что затрудняется прокатка.
При добавке 0,1—0,2 % Ti уменьшается зерно, повышается темпера-тура рекристаллизации и уменьшается анизотропия механических свойств.
Температура горячей обработки 150—200 °С, отжиг 50—100 °С. Температура начала рекристаллизации 20 °С. Максимальная допустимая (суммарная) деформация в горячем состоянии 96 %.
Примерное назначение цинка:
—для производства химически чистых реактивов; для нужд электротехнической промышленности и для научных целей;
— для нужд полиграфической и автомобильной промышленности;
—для отливаемых под давлением особо ответственных деталей авиа и автоприборов; для изготовления оксида цинка, применяемого в химико-фармацевтической промышленности; для химически чистых реактивов; для получения цинкового порошка, используемого в производстве аккумуляторов;
—для листов, применяемых в производстве гальванических элементов; для отливаемых под давлением ответственных деталей авиа- и автоприборов; для изготовления цинковых сплавов, обрабатываемых давлением; для горячего и гальванического оцинкования изделий и полуфабрикатов; для изготовления высококачественных сухих цинковых белил; для изготовления цинкового порошка; для легирования алюминиевых сплавов;
—для производства листов; для медно-цинковых сплавов и бронз; для изготовления проволоки для металлизации; для горячего оцинкования изделий и полуфабрикатов; для изготовления цинкового порошка, применяемого в химической и металлургической промышленности;
Значительное количество цинка идет на оцинкование железа и сплавов на его основе в целях предохранения их от коррозии. Цинк используется для получения сплавов с медью (латуни), с медью и оловом (бронзы), с никелем (мельхиор), с медью и никелем (нейзильбер), а также для изготовления подшипниковых сплавов (типа ЦАМ).
Широкое применение нашли изделия, получаемые литьем под давлением (авиационная, автомобильная и другие отрасли промышленности),
В последние годы цинк используют в космической технике (покрытия стартовых конструкций для запуска ракет, краска из сульфида цинка для покрытия космических кораблей). Сульфид цинка используется для обнаружения a-, b- и g- радиации, а цинксеребряные оксидные батареи вследствие высокой мощности (в 5—6 раз большей, чем мощность лучших батарей других типов) служат в качестве источников энергии в космических кораблях.
Антимонид цинка используют в качестве полупроводника, оксид цинка — при производстве резины и ее обработке, при производстве краски (цинковые белила).
Цинк применяют также для изготовления медицинских препаратов.
Характеристика рудного цинкового сырья
В природе цинк встречается главным образом в виде сульфида и в меньшей степени—в виде кислородных соединений. В соответствии с преобладающими минералами цинковые руды делят на сульфидные и окисленные. Наибольшее промышленное значение имеют свинцово-цинковые сульфидные полиметаллические руды, содержащие, кроме цинка и свинца, также медь, кадмий, благородные и редкие металлы. Рост масштабов добычи и производительности используемой при этом техники потребовал массовых обрушений горной массы, что вызывает разубоживание добытой руды за счет захваченной попутно пустой породы. Истощение запасов богатых руд заставляет вовлекать в разработку более бедные руды сложной структуры, что также ведет к получению бедного металлургического сырья. Основным способом первичной переработки сульфидных свинцово-цинковых руд является селективное флотационное обогащение с получением цинкового, свинцового, а иногда медного и пиритного концентратов.
Рудные залежи разнообразны по структуре. Обычно залежи сплошных сульфидных руд перемежаются более или менее значительными зонами вкрапленников, а в верхней части переходят в зону окисленных минералов. Сульфидные руды содержат цинк главным образом в форме сфалерита (низкотемпературная модификация ZnS), а иногда в форме вюрцита (высокотемпературная модификация ZnS). Железистые разновидности ZnS называют марматитом. Содержание железа в марматите существенно влияет на извлечение цинка из сырья при гидрометаллургическом производстве цинка. В окисленных цинковых рудах цинк представлен главным образом в форме карбонатов (смитсонит ZnCO3 и гидроцинкит ZnCO3 • 3 Zn(OH)2 с изоморфными примесями железа и меди) и силикатов (виллемит Zn2SiO4 и каламин Zn4(OH)2, [Si2O7] • Н2О).
Извлечение цинка в цинковый концентрат обычно составляет 70—85 % от содержания в сульфидных свинцово-цинковых рудах. Содержания технологических важных компонентов в цинковых концентратах обычно укладываются в следующие пределы, %: Zn 40-60; Pb 0,2-3,5; Сu 0,15-2,3; Fe 2,5-13; S 30-35; Cd 0,1-0,5; As 0,03-0,3; Sb 0,01-0,07; Co 0,001-0,013; In 0,001-0,07. Дисперсность концентратов обычно такова, что верхний предел крупности 300 мкм, в том числе фракция -75 мкм составляет 35-50 %, но из тонкодисперсных руд концентраты имеют верхний предел крупности 100 мкм и содержат 70-90% фракции - 75 мкм.
Основные способы извлечения цинка из сырья
Сульфидное цинковое сырье можно подвергнуть прямому восстановлению с получением металлического цинка, например, по реакции ZnS + H2↔ Zn + H2S.
Однако даже такие активные восстановители, как Н2 и СО, при весьма высоких температурах неэффективны. Практически рациональней проводить раздельно окисление ZnS и восстановление окисленного цинка до металла.
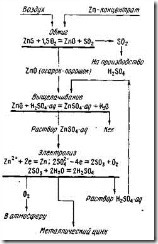
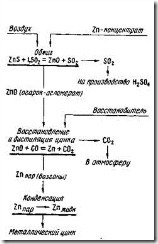
В промышленности окисление ZnS с получением ZnO проводят пирометаллургическим способом, т.е. в газовой среде при высоких температурах. Восстановление цинка из ZnO проводят или пирометаллургическим, или гидрометаллургическим способом. Последний состоит в том, что водный раствор ZnS04 • aq, полученный кислотным растворением ZnO, подвергают электролизу. В зависимости от способа восстановления окисленного цинка различают пирометаллургическое и гидрометаллургическое получение цинка. Технологические схемы того и другого способов представлены на рис. 75 и 76. Эти схемы предельно упрошены и отражают лишь принцип технологий.
Промышленные способы получения цинка из сульфидных концентратор обусловлены свойствами ZnS, ZnO и цинка. Сульфид и оксид цинка тугоплавки. Так, ZnS при атмосферном давлении возгоняется при t ≥ 1200°С, но не плавится вплоть до 2000 С, a ZnO плавится при t ≈ 1975°С. Поэтому окисление ZnS с получением ZnO можно вести е большой скоростью благодаря сохранению дисперсного твердого состояния материала яри высоких температурах (развитость поверхности контакта взаимодействующих фаз). Процесс окисления ZnS экэотермичен и при достаточно высоких температурах не требует топлива (скорость тепловыделения достаточна для поддержания температуры за счет тепла реакции) и даже позволяет использовать процесс как источник энергии.
|
|
|
|
Рис. 75. Технологическая схема пирометаллургического получения цинка |
Рис. 76. Технологическая схема гидрометаллургического получения цинка |
Восстановление цинка из оксида требует больших затрат энергии. Поэтому пирометаллургическое восстановление осуществляют при высоких температурах и концентрациях СО (восстановитель). Электролитическое восстановление также связано с большим расходом электроэнергии, а напряжение выделения цинка значительно выше, чем для других тяжелых цветных металлов. Металлический цинк легкоплавок (tпл =419°С) и летуч (tкип = 907°С при атмосферном давлении), поэтому в условиях термического восстановления цинка из ZnO образуется парообразный металлический цинк. Рассмотрим особенности пиро- и гидрометаллургического способов получения цинка.
При пирометаллургическом способе (см. рис. 75) в конечном счете получают огарок в виде пористых и прочных кусков, т.е. агломерата. Обжиг ведут так, чтобы материал сначала терял в результате окисления серу, а затем спекался. Для спекания материала необходимо, чтобы в слое развивалась температура 1300—1400°С. Пористость и кусковатость агломерата обеспечивают ему необходимую газопроницаемость для последующего углетермического восстановления цинка. Восстановителем служит газифицированный углерод (СО). Процесс ведут с отгонкой образующегося парообразного металлического цинка (дистилляция). При этом расходуется значительное количество высококачественного топлива.
При гидрометаллургическом получении цинка (см. рис. 76) обжиг ведут с получением огарка-порошка при 900—1000°С. Высокая дисперсность огарка способствует быстрому и полному выщелачиванию его в растворе H2SO4. Раствор ZnS04• aq подвергают электролизу, при котором восстанавливается цинк и регенерируется кислота для повторного использования в качестве растворителя ZnO из огарка.
Обжиг цинковых концентратов был и остается основным способом окисления сульфидного сырья.
Как видно из предельно упрощенной технологической схемы каждого способа (см. рис. 77 и 78), получение цинка из минерального сырья требует ряда последовательных стадий (переделов). Но реальная технология получения цинка гораздо сложней. Это объясняется двумя основными причинами: 1) необходимостью отделять от цинка целый ряд сопутствующих ему в сырье компонентов; 2) необходимостью физически подготавливать сырье и промежуточные продукты для последующих стадий переработки.
При более детальном рассмотрении способов, можно выделить их разновидности, которые в основном различаются способом и устройством для восстановления и дистилляции цинка: 1) в горизонтальных ретортах; 2) в вертикальных ретортах; 3) в электрических печах; 4) в шахтных печах. Для разных аппаратов требуется разное состояние и свойства агломерата, что обусловливает специфику способов агломерации.
Гидрометаллургическое получение цинка (рис, 76) имеет разновидности, различающиеся в основном способами выщелачивания огарка: 1) растворение только легко растворимых форм цинка (остаток от выщелачивания - цинковый кек - перерабатывают пирометаллургически); 2) полное растворение всех форм цинка из огарка. Эти разновидности технологии различаются способами разделения цинка и железа, что имеет принципиальное значение в гидрометаллургии цинка. При обжиге концентратов значительная часть цинка связывается с железом в труднорастворимый феррит ZnFe2O4. При неполном выщелачивании цинка из огарка феррит цинка остается в кеке. Благодаря этому отделяют основную часть железа от цинка, не переводя железо в раствор. При полном выщелачивании цинка из огарка железо переходит в раствор, а затем избирательно осаждается. Оборудование для различных вариантов гидрометаллургии цинка в основном однотипное и конструктивно простое. Если сопоставить пирометаллургическое и гидрометаллургическое получение цинка, то можно сделать следующее заключение. Главное и немаловажное преимущество пирометаллургии состоит в компактности основной аппаратуры благодаря высокой удельной производительности аппаратов. Недостатками метода являются высокие расходы на топливо, ремонт оборудования, подготовку материалов к основным операциям, обезвреживание технологических газов перед выбросом в атмосферу.
Гидрометаллургическое получение цинка имеет ряд преимуществ перед пирометаллургическим: 1) большие возможности полно и комплексно перерабатывать сырье; 2) с большой рентабельностью применим к бедному и сложному сырью; 3) используется удобный вид энергии - электрический; 4) требует меньших удельных затрат энергии; 5) легче осуществимы природоохранные меры; 6) лучше условия труда; 7) доступней механизация и автоматизация процессов; 8) получается цинк лучшего качества.
Перечисленные преимущества гидрометаллургии цинка особенно важны в современных условиях, когда обострился энергетический кризис, ужесточились экологические ограничения, потребовалось улучшение условий труда и сокращение ручного труда, возросла необходимость полно и комплексно использовать сырье, которое становится бедней, сложней и дороже (стоимость цинкового концентрата достигает 65 % от общих затрат на производство цинка).
Исторически сложилось, так, что промышленное получение цинка началось пирометаллургическим способом и осуществлялось в горизонтальных ретортах. При всем несовершенстве этого способа более ста лет он был единственным. Гораздо позже, когда появилась возможность осуществить промышленный электролиз, начали применять гидрометаллургический способ.
В металлургии цинка в качестве исходных материалов используют не только минеральное и вторичное сырье, но также и цинксодержащие продукты других производств: шлаки и пыли металлургических производств свинца, меди, олова, чугуна. Эти продукты гораздо бедней по цинку, чем цинковые концентраты.
Цинковистые шлаки до недавнего времени считались отвальными продуктами, хотя в них содержится значительное количество цинка, особенно в свинцовых шлаках (10—17 % Zn).
Жидкие шлаки перерабатывают путем продува их пылегазовой смесью воздуха с углеродсодержащими материалами (пылеуголь, мазут и др.). Этот способ называют фьюмингованием. Из твердых шлаков окисленный цинк восстанавливают коксиком в трубчатых вращающихся печах - вельц-печах. Этот способ называют вельцеванием. Вельцевание применяют также для переработки цинкового кека (остаток от неполного выщелачивания цинка из огарка). Цинк, отогнанный при фьюминговании и вельцевании, конденсируют в виде ZnO, а возгоны перерабатывают гидрометаллургически.
Цинковые кеки являются массовым продуктом гидрометаллургии цинка. Переработка цинковых кеков в мире так распределяется по методам, % гидрометаллургическим (полное выщелачивание цинка) 55; свинцовой шахтной плавкой с фьюмингованием шлаком ~ 25 (в основном заводы США и Канады); вельцеванием и электротермией ~ 20 (заводы Японии). В России основным способом переработки кеков пока остается вельцевание.
Цинксодержащие пыли металлургических производств являются ценным сырьем: кроме цинка, в них содержится ряд редких металлов (In, Se, Те,, Ge и др.). Но вместе с ценными металлами в пылях концентрируются и вредные примеси (As, Sb, Cl, F). Переработка пылей должна быть комплексной. Это сложная технологическая задача, которая не нашла пока оптимального решения.
Обжиг цинковых сульфидных концентратов
Главная цель обжига концентрата — быстрей, полней и с наименьшими затратами превратить сульфидный цинк в оксидный, из которого цинк рациональней восстанавливать. При этом огарок надо получить в таком состоянии, чтобы он был наиболее благоприятен для осуществления последующих стадий технологии и в конечном счете обеспечил высокие технико-экономические показатели производства в целом. Кроме того, желательно полнее утилизировать образующийся при обжиге S02 и выделяющееся тепло.
Обжиг концентратов ведут с получением огарка-порошка и огарка-агломерата для последующей переработки соответственно гидро- или пирометаллургическим способом.
Огарок, предназначенный для выщелачивания, должен удовлетворять следующим требованиям: 1) иметь достаточно низкое содержание сульфидной серы (< 0,1-0,3 %); 2) умеренное содержание растворимых сульфатов (![]() ≤ 2—4 %); 3) высокое содержание мелкой фракции (—0,15 мм); 4) умеренное содержание ферритного и силикатного цинка. В современной практике огарок-порошок для выщелачивания получают в печах кипящего слоя (КС) при 900—1000°С (преимущественно при 950-970°С).
≤ 2—4 %); 3) высокое содержание мелкой фракции (—0,15 мм); 4) умеренное содержание ферритного и силикатного цинка. В современной практике огарок-порошок для выщелачивания получают в печах кипящего слоя (КС) при 900—1000°С (преимущественно при 950-970°С).
Цинковый агломерат должен удовлетворять следующим требованиям: 1) быть достаточно пористым и прочным; 2) иметь достаточно низкое содержание сульфидной серы (< 1%); 3) после дробления иметь определенную крупность (~4—12 мм, причем мелкая фракция лишь вдвое отличается размером от крупной).
В современной практике пирометаллургического производства цинка - обжиг концентратов проводят в две стадии. На 1-й стадии концентрат обжигают на порошок с частичной или почти полной десульфуризацией в печах КС при 1050-1100°С. На 2-й стадии этот огарок подвергают агломерационному обжигу на агломашинах (максимальная температура 1300— 1400°С).
Химизм процессов обжига
Под химизмом процессов подразумевается совокупность химических превращений, происходящих в определенной последовательности в результате взаимодействия исходных веществ. Химизм процесса характеризуется первичными, промежуточными и конечными продуктами превращений. В соответствии с этим последовательные реакции делят на первичные, вторичные и т.д., а продукты этих реакций называют первичными, вторичными и т.д.
Итак, первичные реакции окисления сульфидов могут быть трех типов:
MeS + 2 02 = MeSO4 (8.1)
MeS + 1,5 О2 = МеО + SO2 (8.2)
MeS + 02 = Me0 + SO2 (8.3)
Вторичные реакции окисления сульфидов можно разделить на три типа: 1) реакции окисления низших оксидов металла и серы до высших (развитие окисления компонентов сульфида); 2) взаимодействие оксидов серы и металла (сульфатообразование); 3) взаимодействие оксидов металлов между собой и с кремнеземом (феррито- и силикатообразование).
Рассмотрим конкретные и наиболее важные для технологии превращения, происходящие при обжиге цинковых концентратов. Хотя технологические режимы охватывают узкие интервалы режимных параметров, рассмотрим химизм процессов в более широком диапазоне условий, чтобы представить последствия отклонения от принятых в практике режимов.
Сульфид цинка встречается в концентратах в двух модификациях: распространенная - сфалерит α-ZnS и более редкая — вюрцит β-ZnS. При нагреве переход α↔β происходит при 1020°С, при более низких температурах β -ZnS существует как метастабильный. Химизм окисления этих модификаций одинаков.
Выше отмечалось, что ZnS при атмосферном давлении не плавится, а при t >1200°C сублимирует. В природных ZnS всегда содержится изоморфная примесь Fe2+ (обычно в пределах 3-10 %) и микропримеси (Mn, Cd, Tl, Hg, In).
Установлено, что от температуры начала заметного окисления сфалерита и до 900°С первичным твердым продуктом окисления является ZnO. Следовательно, при t < 900-1000°С окисление ZnS идет по реакции
ZnS + 1,5 О2 = ZnO + S02. (8.4)
Однако при больших температурах обнаруживается возгонка материала при обжиге ZnS. Причем чем интенсивней окисление ZnS за счет повышения t и ![]() , тем больше дебаланс между убылью количества ZnS и прибылью количества ZnO в обжигаемых образцах. Это обусловлено протеканием окисления по реакции
, тем больше дебаланс между убылью количества ZnS и прибылью количества ZnO в обжигаемых образцах. Это обусловлено протеканием окисления по реакции
ZnSтв+02 =Znnap +S02. (8.5)
Далее пары цинка окисляются. Реакция (8.5), вероятно, является суммарной и включает диссоциацию ZnS на Zn° и S2.
Изоморфное железо при окислении (Zn, Fe)S сразу образует ZnFe2O4. Феррит цинка, полученный при температуре меньше 1000°С, практически немагнитен и плохо растворим в растворах H2S04.
В окалине на зернах сфалерита сульфатная сера обнаруживается во внешней части, удаленной от поверхности сульфидного ядра. Это свидетельствует об образовании сульфатов цинка в результате взаимодействия ZnO с S03 (вторичные сульфаты). При этом образуются или ZnS04, или ZnO*2 ZnS04. На воздухе в изотермических условиях ZnSO4 устойчив до 670°С, a ZnO • 2 ZnS04 - до 760°С. При наличии в газовой фазе S03 эти сульфаты не диссоциируют и при более высоких температурах. Сульфатизации подвержен не только оксид цинка, но и феррит цинка, т.е. сульфатизация цинка снижает его ферритизацию. Таким образом, вторичные сульфаты цинка в зависимости от температуры и ![]() образуются по реакциям
образуются по реакциям
ZnO + S03 = ZnSO4, ZnFe204 + SO3 = ZnS04 + Fe2O3 (8.6a)
или 3 ZnO + 2 SO3 = ZnO * 2 ZnSO4, (8.6б)
3 ZnFe2O4 + 2 S03 = ZnO*2ZnS04 + Fe203. (8.6в)
Ферритизация цинка возможна и в результате взаимодействия ZnO с Fe203, образовавшимся от окисления отдельных зерен сульфидов железа. Степень протекания тонкой ферритизации зависит от условий обжига: повышение температуры при обжиге и наличие сростков зерен ZnS и FeS2 способствуют ферритизации цинка.
Для гидрометаллургической переработки огарков имеет значение влияние условий обжига на растворимость феррита цинка. Чем мельче феррит, несовершенней его кристаллическая структура, неизометричны и пористы зерна, тем легче он поддается кислотному растворению.
Технологически опасны кислоторастворимые силикаты. В цинковом огарке таким силикатом является Zn2Si04.
В условиях КС образование Zn2Si04 при обжиге цинковых концентратов - результат наличия сростков ZnS с породообразующими минералами, спекания соударяющихся зерен. При высокотемпературном обжиге (t > 1000°C) частичная отгонка цинка в результате реакции (8.4) с последующей конденсацией окислившегося цинка на силикатных фазах способствует усилению образования Zn2 Si04. Аналогичным образом усиливается и ферритизация цинка.
В цинковых концентратах, кроме сфалерита, обычно содержатся в заметных количествах другие сульфиды: PbS, CuFeS2, FeS2.
Халькопирит претерпевает следующие превращения. В результате более быстрого окисления железа по сравнению с медью периферия зерен CuFeS, обедняется железом и превращается в борнит (медножелезный сульфид переменного состава, в котором меди больше, чем железа). В продуктах окисления CuFeS, содержатся Сu0 , Сu2О, СuО, CuFe2O4, CuSO4 и CuO·CuSO4. Реакции, приводящие к образованию этих продуктов, понятны в свете изложенного выше.
Пирит диссоциирует с образованием элементарной серы (окисляющейся в газовой фазе до S02 и SO3 и пирротина (FeS1 +x, где О < х < 0,38). Пирротин окисляется до Fe3О4 и далее до конечного продукта Fe2О3.
Из этого следует, что основные компоненты в огарке представлены следующими фазами; цинк в виде ZnO, ZnFe2O4, ZnSO4, ZnO·2ZnSO4, Zn3SiO4, ZnS; железо в виде Fe304Fe203; ZnFe304; свинец в виде PbSO4, PbO· PbSO4, 2PbO·PbSO4, РbО Pb2Si04 PbS; медь в виде CuFe,O4, CuSO4, CuO·CuSO4 Cu2S, борнита Cu2O и Cu0. Для достижения низких содержаний сульфидной серы в огарке неблагоприятно сочетание заметных количеств сульфидов меди и свинца в концентрате из-за образования легкоплавкой эвтектики PbS – Cu2S (борнит), у которой tпл =540°C.
Обжиг цинковых концентратов для выщелачивания
Принцип обжига в КС и его достоинства
Достоинства этого способа обжига являются следствием сжигания концентрата, приведенного в особое состояние псевдоожижения. Рассмотрим суть и условия создания этого состояния.
Непосредственно после перехода в псевдоожиженное состояние слой сохраняет однородность и спокойную поверхность. С ростом ω расширение слоя вызывает образование газовых пузырей (нарушается однородность), повышается интенсивность перемешивания зерен и появляются колебания поверхности слоя и всплески (рис. 78, в). Если спокойный слой шихты слишком высок по отношению к диаметру печи, то восходящие пузыри в КС сливаются и укрупняются. В пределе это может привести к образованию воздушных пробок но всему сечению слоя, которые чередуются с движущимися поршнями псевдоожиженной шихты. Образование пузырей вызывает малые колебания давления дутья, которые возрастают с увеличением размера пузырей. Укрупнению пузырей способствует укрупнение монодисперсного порошка. Полидисперсность порошка сглаживает пульсации давления. Обычно слишком мелкие фракции огарка выносятся из КС, а слишком крупные оседают на подину. В КС огарок удерживается в определенном диапазоне дисперсности.
Печь КС - непрерывно действующий реактор почти идеального перемешивания. В таких реакторах обновление материала в слое замедляется пропорционально степени обновления.
Материал в кипящем слое текуч, интенсивно перемешивается, что обеспечивает однородность слоя по составу и температуре. Обжиг концентратов в КС имеет многие преимущества перед ранее применявшимися способами: 1) высокая производительность (удельная производительность по площади пода в 3-4 раза выше, чем в многоподовых печах, и в 1,5-2 раза выше, чем при обжиге во взвешенном состоянии); 2) стабилизация режима обжига и повышение качества огарка (содержание сульфидной серы в огарке из печи кипящего слоя 0,1-0,3 % вместо 0,2-0,5 % при обжиге во взвешенном состоянии или 0,3-1,0 % при обжиге на подах); 3) повышение ![]() в газах (это улучшает их утилизацию на получение H2SO4); 4) автотермичность с высокой степенью утилизации технологического тепла; 5) упрощение подготовки шихты и обслуживания печи (возможность полной механизации, автоматизации, увеличение длительности кампании печей КС).
в газах (это улучшает их утилизацию на получение H2SO4); 4) автотермичность с высокой степенью утилизации технологического тепла; 5) упрощение подготовки шихты и обслуживания печи (возможность полной механизации, автоматизации, увеличение длительности кампании печей КС).
Это способствует быстрому распространению и широкому применению обжига в КС.
Общая схема цепи аппаратов
Технология обжига цинковых концентратов для выщелачивания на разных заводах не имеет принципиальных различий: обжиг ведется в печах КС в одну стадию. Различия касаются следующего: 1) способов подготовки и исходного состояния шихты для обжига; 2) конструкции печей КС; 3) подготовки и транспорта огарка для выщелачивания; 4) температурных и концентрационных условий обжига; 5) способов утилизации тепла печей КС.
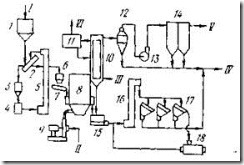
Рис. 79. Схема цепи аппаратов обжигового цеха (I - V - потоки): I - исходная шихта; II- воздух; III - вода; IV - огарок на выщелачивание; V — SO2 на производство Н2SО4; 1 - бункер для шихты; 2 - вибрационный грохот; 3 - бункер для комков шихты; 4 - дезинтегратор; 5 - элеватору б - бункер для мелкой шихты; 7 - ленточный питатель; 8 - печь КС; 9 - турбовоздуходувка; 10 - стояк с кессонами испарительного охлаждения; 11 - барабан-сепаратор пароводяной смеси; 12 циклон; 13 - дымосос; 14 - электрофильтры; 15 - водоохлаждаемый аэрохолодильник (для охлаждения" огарка); 16 - элеватор; 17- вибросита; 18 - шаровая мельница
На рис, 79 показана схема цепи аппаратов обжигового цеха. Схема включает узел подготовки шихты к обжигу в сухом виде, печь КС, узел теплоотъема тепла из газа в стояке и из КС кессонами испарительного охлаждения, узел пылеулавливания циклоном и электрофильтрами, узел подготовки огарка к выщелачиванию в сухом виде, узел гидродинамического обеспечения технологического тракта (воздуходувка и дымосос).
Приготовление шихты
На цинковых заводах обычно перерабатывают смесь концентратов, отличающихся по составу. При шихтовке концентраты смешивают в пропорциях, отвечающих определенному составу шихты по цинку, сопутствующим полезным и вредным компонентам. Состав шихты должен удовлетворять условиям, обеспечивающим достижение целей обжига.
Шихту в печь КС подают в сухом виде или в виде пульпы. Подачу на обжиг сухой шихты применяют для шихт, образованных из привозных и довольно близких по составу концентратов. Шихта в виде пульпы предпочтительна, когда цинковый завод находится рядом с обогатительной фабрикой, снабжающей завод концентратом, или когда в шихту идут сильно различающиеся по составу концентраты (в состоянии пульпы шихта проще и лучше перемешивается). Однако загрузка пульпы в КС увлажняет отходящие газы, и это усложняет их переработку, усиливает коррозию оборудования и газоотводящих систем. Пульпу сложней, чем сухую шихту, равномерно распределить по кипящему слою.
Для получения сухой шихты концентраты грейферным краном смешивают для однородности материала. Далее шихту подсушивают в сушильном барабане до остаточной влажности 6—8%. Если концентраты достаточно сухие, то подсушка не требуется. Подсушенную шихту измельчают на дисковых истирателях или на дезинтеграторах и отсеивают крупные комки на грохотах.
Шихту в виде пульпы готовят репульпацией смеси концентратов водой (в пульпе 75—80% твердого) и дополнительно перемешивают в баках с мешалками.
Типы аппаратурного оформления обжига в КС
Конструктивно печи КС разнообразны и различаются профилем поперечного сечения (круглые и прямоугольные), величиной отношения надслоевого объема печи v к площади пода S, способом загрузки шихты в печь (через форкамеру и в слой или через загрузочные окна в стенках печи и по всей поверхности кипящего слоя), конструкцией воздухораспределительной подины.
На рис. 80 схематически показана цилиндрическая печь КС наиболее распространенной на отечественных заводах конструкции. Площадь пода печи 34 м2, площадь форкамеры ~1,5 м2, высота печи 10 м, высота сливного порога 1,0- 1,2. Форкамера служит для загрузки шихты в КС, а сливной порог - для выгрузки огарка.
Очень ответственным элементом конструкции печи является воздухораспределительная подина. Подину печи выполняют из жароупорного бетона на стальном перфорированном листе с вставленными в отверстия соплами для распределения дутья равномерно по площади. Площадь сечения отверстий в соплах по отношению к площади пода (живое сечение) составляет 0,8-1,0%. В форкамере сопла расположены чаще и воздуха на единицу площади подают больше для предотвращения залегания загруженной шихты на подину.
Тонкие (пылевидные) фракции выносятся с дутьем из КС и обжигаются во взвешенном состоянии. Пылевая часть огарка улавливается в пылеуловителях и выгружается из них для выщелачивания. Грубодисперсная часть огарка выгружается из печи через сливной порог и тоже направляется на выщелачивание.
Для стационарного теплового режима обжига необходим тепловой баланс в КС, который обеспечивается отводом тепла из слоя, % с обжиговыми газами 60, с огарком, с пылью и через стенки печи 20. Остальное тепло надо отводить специальными средствами, чтобы избежать перегрева в слое. Обычно это осуществляют трубчатыми кессонами испарительного охлаждения. Отъем тепла из обжиговых газов осуществляют с помощью котлов-утилизаторов или вертикальных стояков, охлаждаемых кессонами испарительного охлаждения. Котлы-утилизаторы более сложны конструктивно, но они дают пар с высокими параметрами (400-565°С и 4,5-6,0 МПа) в количестве 1,1-1,4 т/т обжигаемого концентрата. При этом используется до 55 % технологического тепла, остальное теряется с огарком и пылью, через стенки печи и с газом, отправленным на производство H2SO4. Кроме того, котлы-утилизаторы являются эффективными пылеуловителями (пылеулавливание 90-95 %), что осложняет их эксплуатацию, так как теплообменные поверхности зарастают пылевыми отложениями. Стояки испарительного охлаждения конструктивно просты, надежны в эксплуатации, но обеспечивают меньший теплотъем от газов в виде пара в количестве 0.85 0.92 т/т обжигаемого концентрата, пар более низких параметров (110°С и 0,6 МПа), чем в котле-утилизаторе. Надежность стояков в работе обусловлена сведением к минимуму оседания пыли в них. Пар из кессонов, обеспечивающих теплоотъем из КС, выводится или на котел-утилизатор, или на барабан-сепаратор, комплектующий теплоотнимающий стояк.
Узел пылеулавливания состоит из котла-утилизатора (если он включен в систему пылегазового тракта), одной или двух ступеней циклонов для грубого пылеулавливания и электрофильтров для тонкого пылеулавливания. Обеспыленный газ направляют в сернокислотное производство.
Дутье воздуха в печь подают от турбовоздуходувки по воздуховодам в воздушную коробку, расположенную под воздухораспределительной подиной. А далее воздух через сопла в подине под определенным давлением поступает в КС. Производительность воздуходувки выбирают из расчета, что теоретически необходимое для обжига количество воздуха составляет 1500-1600 м3/т концентрата, но необходим избыток воздуха на 20-30 % (коэффициент избытка воздуха а = 1,2*1,3). Таким образом, удельный расход воздуха составляет около 2000 М3/т шихты. Скорость дутья должна быть ω = 10÷1З см/с. Тяговый режим в газоотводящем тракте должен обеспечить отсос всех отходящих из печи газов с учетом незначительного подсоса воздуха на участке печь - эксгаустер (дымосос).
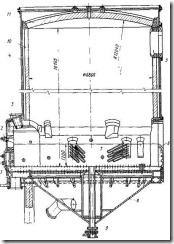
Рис. 80. Цилиндрическая печь кипящего слоя:
1 - подина; 2 — форсунка для розжига печи; 3 - форкамера для загрузки концентрата; 4 — корпус печи; 5 — отверстие для отвода газов; 6 — сливной порог; 7 — трубчатые кессоны испарительного охлаждения; 8 - воздушная коробка; 9 - задвижка с пневмоприводом; 10 - футеровка; 11 - свод
Транспортировку огарка от печей КС осуществляют или в виде пульпы, или в сухом виде. Транспортировка пульпы аппаратурно проще, чем сухого огарка. Но транспорт пульпы имеет ряд серьезных недостатков: 1) отсутствие буферного склада огарка перед цехом выщелачивания; 2) отсутствие весового контроля огарка, поступающего на выщелачивание; 3) усложнение схемы выщелачивания операциями гидроклассификации огарка и обработки песковой фракции. Эти недостатки менее значимы при непрерывном выщелачивании огарка и только в этом случае применим гидротранспорт огарка. Отмеченные недостатки гидротранспорта огарка объясняют предпочтение в мировой практике транспортировки от печей КС сухого огарка. В этом случае горячий огарок охлаждают либо в водоохлаждаемых холодильниках, либо в аэрохолодильниках с КС. Охлажденный огарок транспортируют водоохлаждаемыми цепными или шнековыми конвейерами, или пневмотранспортом, или после суспендирования в кислых цинковых растворах в виде пульпы по трубопроводам. Сухой огарок подвергают аэросепарации или рассеву на виброситах с последующим измельчением крупной фракции (+0,3 мм) в шаровой мельнице. После измельчения эту часть огарка тоже отправляют на выщелачивание. На некоторых зарубежных предприятиях предпочитают подвергать измельчению весь огарок для исключения сепарации в подготовке огарка к выщелачиванию.
Совершенствование обжигового передела по технико-экономическим показателям достигают также изменением конструкции печей КС. Эти изменения направлены на увеличение единичной мощности печей (до 550-800 т/сут) за счет увеличения площади пода (до 72-123 м2). Повышение единичной мощности оборудования снижает эксплуатационные расходы, повышает производительность труда. В ряде случаев предприятия не имеют запасных обжиговых печей или даже работают на единственной крупнотоннажной печи. Поэтому на период ремонта печи или сернокислотной установки, потребляющей обжиговый газ, предусмотрено хранение запаса огарка в специальных хранилищах, из которых он поставляется на выщелачивание.
Интенсификация обжига за рубежом достигается увеличением высоты печных камер (до 12-17 м) и расширением верхней части печи (в 1,3-1,5 раза), т.е. за счет увеличения отношения надслоевого объема печи v к площади пода S, которое достигает 20-25. Это позволяет повысить скорость дутья в КС при малой скорости газа в надслоевом пространстве и умеренных избытках воздуха. Благодаря высоким значениям отношения v/S ограничен пылеунос, a ![]() в газах значителен (см. ниже).
в газах значителен (см. ниже).
Увеличение площади пода печей потребовало изменить способ загрузки шихты в печь КС для лучшего ее использования: вместо загрузки шихты через форкамеру в слой применяют загрузку скоростными забрасывателями через загрузочное окно в стенке печи для равномерного распределения шихты по поверхности КС.
Практика обжига в печи КС
Для поддержания нормального режима обжига в печи КС необходимы следующие условия: а) постоянство минералогического и дисперсного состава шихты и скорости загрузки ее в слой; б) равномерное распределение дутья по площади подины; в) постоянство заданного давления в воздушной коробке под подиной; г) постоянство тягового режима в пылегазовом тракте для отвода технологических газов.
Перечисленные выше условия направлены главным образом на создание равномерного и устойчивого псевдоожижения. В производстве нормальное состояние кипящего слоя создается при давлении дутья 15 - 16кПа, из них 4 - 6 кПа приходится на преодоление гидравлического сопротивления подины печи. Следовательно, гидравлическое сопротивление КС должно составлять ~ 10 кПа. Такое давление должен создавать спокойный слой огарка на подине, а это соответствует ~ 1 т/м2 (в согласии с практикой загрузки печи огарком при ее запуске).
Для нормальной работы системы теплоотъема и пылеулавливания серьезные помехи создают пылевые отложения в пылегазовом тракте. Повышение ![]() в отходящих газах вызывает сульфатизацию и упрочнение этих пылевых отложений, что затрудняет их удаление. Сульфатизация отложений становится возможной по мере охлаждения пыли.
в отходящих газах вызывает сульфатизацию и упрочнение этих пылевых отложений, что затрудняет их удаление. Сульфатизация отложений становится возможной по мере охлаждения пыли.
Влияние условий обжига на технологические показатели процесса
Важнейшими технологическими показателями обжига являются следующие: 1) производительность; 2) распределение обжигаемой шихты по продуктам обжига (огарок и пыль); 3) концентрация SO2 в технологических газах; 4) качество огарка (дисперсность и содержание сульфидной серы, растворимых сульфатной серы и цинка, кремнезема и железа).
Рассмотрим условия и их влияние на эти показатели обжига.
Производительность. Обжиг цинкового концентрата в теплотехническом отношении является сжиганием высокозольного топлива. Если сульфидные зерна крупные, то на них образуется толстый слой окалины и горение будет протекать во внутридиффузионной области. В этом случае внешними воздействиями скорость горения не повысишь. Но если зерна сульфида умеренной крупности (характерной для флотационных концентратов), то, при 950°С горение протекает во внешнедиффузионной области до полного окисления зерен, т.е. скорость горения ограничена молекулярной диффузией 02 через газовую пленку вокруг горящих зерен. Чем больше градиент концентрации 02 во внешнедиффузионном слое, тем выше скорость горения. Величину grad ![]() можно повысить или уменьшением толщины диффузионного газового слоя в результате повышения скорости газа относительно зерен сульфида, или увеличением
можно повысить или уменьшением толщины диффузионного газового слоя в результате повышения скорости газа относительно зерен сульфида, или увеличением ![]() в дутье (обогащение воздуха кислородом). Скорость газа относительно зерен наибольшая в кипящем слое, наименьшая — в спокойном слое, омываемом воздухом по внешней поверхности. Поэтому переход на обжиг в печах КС сразу повысил удельную производительность до 4,8-5,5 т/ (м2 ·сут).
в дутье (обогащение воздуха кислородом). Скорость газа относительно зерен наибольшая в кипящем слое, наименьшая — в спокойном слое, омываемом воздухом по внешней поверхности. Поэтому переход на обжиг в печах КС сразу повысил удельную производительность до 4,8-5,5 т/ (м2 ·сут).
Интенсификация обжига в КС в отечественной практике пошла по пути обогащения дутья кислородом при сохранении дутьевого режима [скорость дутья 10-13 см/с и удельный расход дутья 350-450 м3/(м2·ч)]. Это позволило существенно повысить производительность, так как окисление сульфида во внешнедиффузионной области имеет первый порядок по кислороду [см. уравнение (8.13)]. Практика показала, что рационально повышать ![]() в дутье до 28—32%. При этом достигается производительность 8-10 т/(м2·сут). Дальнейшее обогащение дуля кислородом не целесообразно экономически (прирост производительности уменьшается и не окупает стоимости дополнительно затраченного кислорода) и сложно технически (затруднен достаточно быстрый отъем тепла из КС во избежание чрезмерного перегрева слоя).
в дутье до 28—32%. При этом достигается производительность 8-10 т/(м2·сут). Дальнейшее обогащение дуля кислородом не целесообразно экономически (прирост производительности уменьшается и не окупает стоимости дополнительно затраченного кислорода) и сложно технически (затруднен достаточно быстрый отъем тепла из КС во избежание чрезмерного перегрева слоя).
Интенсификация обжига кислородом привлекает возможностью использовать печи первоначально принятого типа конструкции. В социалистических странах, для которых характерна кооперация производств, применение кислорода как интенсификатора экономически выгодно при комплексном использовании компонентов воздуха, из которого получают как технический кислород, так и N2, Ar, Кг, Хе, Не.
В капиталистических странах был выбран путь интенсификации обжига за счет повышения скорости дутья. Это обусловлено энергоемкостью производства кислорода, что при энергетическом кризисе и трудностях кооперации в использовании побочных продуктов производства кислорода делало нецелесообразным его использование.
Повышение скорости дутья и удельного расхода воздуха [до 600-675 м3/(м2-ч)] усиливает пылеунос из КС. В зарубежной практике при форсированном дутье воздуха выпуск огарка через порог невысок. Это увеличивает долю обжига шихты во взвешенном состоянии и снижает производительность по обожженному материалу, пригодному для выщелачивания, а также влечет другие нежелательные последствия (см. ниже). Чтобы избежать значительного пылеуноса и повысить степень десульфуризации пыли, печи КС делают с большим объемом надслоевого пространства: высокие (до 12-17 м) и расширяющиеся в верхней части (в 1,3-1,5 раза). В результате скорость газа по выходе из КС значительно уменьшается и пыль оседает обратно в КС или дольше витает в надслоевом пространстве и полней окисляется. Температура - наиболее эффективный интенсификатор технологических процессов даже в диффузионной области. Однако повышение t > 970°C при обжиге обычной цинковой шихты нецелесообразно (гранулированную шихту обжигают и при 1000°С). Это вызвано тем, что при более высоких температурах ухудшается качество огарка для последующей гидрометаллургической переработки.
Распределение обжигаемой шихты по продуктам обжига. Технологически важно ограничить унос обжигаемого материала из печи КС в пылегазовый тракт, так как это облегчает теплоотъем и пылеулавливание в пылегазовом тракте.
Обычно на печах отечественной конструкции при t = 950÷970°С выход твердых продуктов составляет, % к их сумме: огарка 65; пыли циклона 30 (при наличии кессонированного стояка в нем осаждается 1/3 этого количества); пыли электрофильтров 3,3; пыли газоходов 1,7. Если температура в слое выше, то выход пыли уменьшается. Если концентрат имеет повышенную дисперсность (получен обогащением тонковкрапленных руд), то выход пыли увеличивается.
Концентрация SO2 в технологических газах. Повышение ![]() в газах улучшает его использование в производстве H2SO4. На воздушном дутье получают обжиговые газы, содержащие 8,5-10% S02 на выходе из печи КС, далее по тракту из-за подсосов воздуха
в газах улучшает его использование в производстве H2SO4. На воздушном дутье получают обжиговые газы, содержащие 8,5-10% S02 на выходе из печи КС, далее по тракту из-за подсосов воздуха ![]() снижается. В зарубежной практике имеются примеры повышения
снижается. В зарубежной практике имеются примеры повышения ![]() добавками элементарной серы в шихту для обжига цинковых концентратов или подачи в дутье печи КС технологических газов агломерирующего обжига свинцовых концентратов. Применение дутья, обогащенного кислородом, повышает
добавками элементарной серы в шихту для обжига цинковых концентратов или подачи в дутье печи КС технологических газов агломерирующего обжига свинцовых концентратов. Применение дутья, обогащенного кислородом, повышает ![]() до 12-15 % в технологических газах на выходе из печи КС.
до 12-15 % в технологических газах на выходе из печи КС.
Качество огарка определяется соответствием его указанным выше требованиям. Чтобы в огарке содержалось не более 0,1—0,3% сульфидной серы, необходимо достичь степени десульфуризации концентрата при обжиге на 99,0—99,7%.
Химизм кислотно-основных взаимодействий при выщелачивании
Для процессов выщелачивания цинкового огарка решающее значение имеет поведение соединений трех компонентов: основного компонента — цинка и примесных компонентов - железа и кремнезема. Вынужденная совмещенность растворения цинка, железа и SiO2 обусловлена образованием между ними соединений ZnFе2O4 и Zn2SiO4 в процессе обжига.
Изменяя кислотность раствора при кислотном выщелачивании цинка, можно одновременно осаждать растворившиеся железо и Si02 и таким образом отделить их от цинка. В основе этих процессов лежат кислотно-основные взаимодействия.
Из соединений, содержащихся в цинковом огарке, легко растворим в воде ZnS04, оксосульфат цинка растворим в воде:
3 (ZnO·2ZnS04)+7H2O=ZnS04 ·3 Zn(OH)2 ·4H2O+5ZnS04·aq.(9.1)
Прочие из перечисленных соединений цинка нерастворимы в воде. В слабокислом растворе (рН < 3) растворимы ZnSO4 · 3Zn(OH)2, ZnO и Zn2SiO4. Для растворения ZnFe2O4 и ZnS с достаточной для практики скоростью необходимы горячие и весьма кислые растворы (t ≥80°C и ![]() > 50 г/дм3).
> 50 г/дм3).
В огарке значительные количества железа содержатся не только в форме феррита цинка, но также в виде Fe2O3, которая столь же плохо растворяется в кислых растворах, как и ферриты. Однако наличие в огарке остатков сульфидной серы, которая выступает восстановителем Fe(III) в оксиде и ферритах, вызывает переход железа и раствор в состоянии Fe(П). Кремнезем в огарке содержится не только и форме Zn2SiO4, но также в форме свободного SiO2 и других породообразующих минералов. Свободный и связанный в породу SiO2 практически не растворяется в растворах Н2S04.
Различие в поведении соединений цинка, железа и кремнезема, содержащихся в огарке, при его выщелачивании используется в технологии. В гидрометаллургии цинка выщелачивают не только огарки, но и окисленные цинковые руды или полученные из них концентраты, в которых, кроме Zn2SiO4 (виллемит), может содержаться Zn4(OH)2(Si207)·H20 (каламин). Последний, как и виллемит, легко растворяется в слабокислых растворах.
Очистку растворов от железа осуществляют в процессе выщелачивания путем гидролитического осаждения, а попутно благодаря соосаждению и от некоторых других примесей (As, Sb и др.).
Гидролиз Fe3+·aq в сульфатном растворе - это взаимодействие его с водой, в результате которого образуются прочные гидроксокомплексы (малодиссоциированные соединения, т.е. слабые основания). Например:
Fe2(SO 4)3· aq + 2 п Н2О= Fе2(OH)2п (SO4 )3-п · aq + п H2SO4 · aq, (9.2)
или в ионной форме
Fe3+·aq + 4 п Н2О = 2 Fe(OH)n(3 - п)+ · aq + 2п Н3О ·aq. (9.3)
Если в кислом растворе нейтрализовать кислоту огарком, то равновесие реакций (9.2) или' (9,3) сдвигается вправо. Это способствует насыщению раствора гидроксокомплексом железа, который начинает выпадать в осадок в виде труднорастворимого гидроксосоединения железа. Осаждение продукта гидролиза путем нейтрализации Н3О+ называется гидролитическим осаждением.
Технологическое значение в гидрометаллургии цинка имеют ярозит R+ Fe3(OH)6(SO4)2, гетит α-FeOOH, гематит α -Fe2O3, а также аморфный основной сульфат 2 Fе2О3·SO3·nH2O.
Основным источником растворимого кремнезема в огарках или окисленных рудах являются силикаты цинка. Кремнезем переходит в раствор в виде ортокремниевой кислоты:
Zn2Si04 + 2H2S04· aq = 2ZnS04· aq + H4Si04· aq, (9.4)
Есть некоторая область кислотностей раствора (рН ≈ 2,0÷3,5), в которой H4Si04 образует истинный раствор. Если смещаться от области существования истинных растворов кремнекислоты в сторону увеличения кислотности (рН 3,5), то последовательно образуются золи, гели, коагели и коагуляты, т.е. коллоидные состояния и продукты их разрушения. Продукты разрушения коллоидных растворов кремнекислот при значительных их количествах ухудшают разделение пульпы и показатели выщелачивания.
Углетермическое восстановление цинка
Восстановление цинка из окисленных материалов в промышленных условиях проводят только углетермически, используя в качестве восстановителя уголь или кокс.
Главная и общая цель этого процесса — отделить цинк от большинства сопутствующих ему компонентов в окисленных промышленных и природных цинксодержащих материалах при наибольших технико-экономических выгодах. Эта цель достигается благодаря тому, что в условиях углетермического восстановления цинк переходит в металлическое состояние, в котором его летучесть гораздо выше летучести других сопутствующих ему компонентов в тех же условиях. Следовательно, при этом происходит избирательная дистилляция цинка, который отгоняется в виде пара. Парогазовую фазу выводят из зоны дистилляции и конденсируют цинк. Если при этом в газовой фазе сохраняется достаточно высокая концентрация СО или конденсация цинка осуществляется достаточно быстро для предотвращения окисления паров цинка, то конденсируется жидкий металл. В противном случае пары цинка окисляются и конденсируется ZnO.
Создать условия для конденсации металлического цинка довольно сложно. Делать это имеет смысл лишь при восстановлении цинка из богатых по цинку окисленных материалов, каким является цинковый агломерат, с получением товарного металла или близкого к нему. Для бедных по цинку материалов (окисленные цинковые руды, продукты металлургического производства — цинковые кеки, цинковистые шлаки и др.) конденсацию отогнанного цинка ведут в окислительных условиях. Полученные при этом возгоны оксида цинка перерабатывают методами, применяемыми для богатых окисленных цинковых материалов, или используют как технический оксид цинка. Таким образом, дистилляция цинка из бедных материалов имеет целью сконцентрировать цинк в малом количестве оксидного возгона.
Пирометаллургическая переработка цинковых кеков в основном проводится методом вельцевания, тогда как в практике других стран большей частью используется свинцовая шахтная плавка (цинковые кеки вводят в шихту агломерирующего обжига свинцового концентрата) с последующим фьюмингованием образующихся при шахтной плавке цинковистых шлаков.
Вельцевание — это восстановление дисперсного твердого цинксодержащего окисленного материала коксиком во вращающихся трубчатых печах с отгонкой металлического цинка и конденсацией окисленного цинка (вельц-оксид).
Агломерированный цинковый огарок с высоким содержанием цинка (до 62 %) подвергают углетермическому восстановлению с дистилляцией и конденсацией металлического цинка в различных агрегатах - горизонтальных и вертикальных ретортах, шахтных и электротермических печах (все в комплексе с конденсаторами). Дистилляцию цинка проводят при 1100-1400°С и при высоких pCO в газовой фазе. Дистилляция цинка из агломерата в горизонтальных ретортах представляет собой периодический процесс, а в прочих (из перечисленных) агрегатах — непрерывный.
Химизм восстановления окисленных цинковых материалов
Для восстановления окисленных цинковых материалов характерно трехфазные протекание процессов и индивидуальное поведение отдельных фаз. Чтобы судить о химизме углетермического восстановления этих материалов, надо знать их фазовый состав.
В цинковых кеках основные компоненты представлены следующими формами: цинк — главным образом ферритом ZnFe2О4 и в малой степени сульфидом ZnS и сульфатом ZnSO4 (за счет захвата сульфатного цинкового раствора); свинец - в основном сульфатом PbSO4 и в малой степени сульфидом; медь и кадмий — главным образом в ферритах; железо находится в форме ферритов, магнетита Fe3O4, аморфного основного сульфата 2 Fe2O3 • SO3 • и Н2О, гематита α-Fe2O3. В процессе сушки влажных кеков, содержащих кислый цинковый раствор, образуются в небольших количествах сульфаты цинка, меди, кадмия (взаимодействие H2SO4 с ферритами).
В твердых цинковистых шлаках цинк находится в следующих фазах: цинксодержащий магнетит (феррифранклинит) (Zn, Fe3+)(Fe3+ Al)2O3, цинксодержащий диортосиликат (цинковый мелилит) [Ca(Zn, Fe2+, Mg)]2 • Si2O, и в малом количестве железистый ортосиликат цинка (железистый виллемит) (Zn, Fe)2 • SiO4. Феррофранклинит и железистый виллемит являются соответственно ферритом и силикатом цинка, в которых понижено содержание цинка против стехиометрических соединений. А в кеках феррит ZnFe2O4 изоморфно содержит кадмий и индий.
В цинковом агломерате цинк находится в следующих формах: цинкита ZnO, феррифранклинита,(Zn, Fe)Fe2О4 железистого виллемита (Zn, Fe)2SiO4. В агломератах для шахтной плавки содержатся значительные количества свинца в форме силикатного свинцового стекла и может быть в небольших количествах в форме феррита свинца РbО (6 — у) • Fe2 О3, где у ≤ 1, как достаточно термически стойкого.
Оксид цинка трудно восстанавливается, и для этого нужны высокие значения pCO и t, при которых процесс идет по реакции
ZnO +CO = Znnap +C02 . (12.1)
Феррит цинка устойчив к диссоциации на воздухе до 1400°С (и до этой температуры он не плавится). Начало его восстановления отмечается при 650—750°С выделением ZnO в самостоятельную фазу и образованием (Zn, Fe)O • Fe203. Это обусловлено тем, что восстановление Fe3+ протекает без попутного восстановления Zn2+ и избыточное количество МеО против стехиометрического количества в шпинели должно выделяться из нее в самостоятельную фазу ZnO, а остаточный феррит сохраняет стехиометрический состав шпинели, но обедняется по цинку, приближаясь к составу Fe3O4. В ограниченной степени возможна реакция
ZnO + (1- х) Fe= ZnFeпар + Fe l-xO (12.2)
Восстановление сульфатов может приводить к образованию сульфида, оксида или металла. Это зависит от соотношения сродства Ме2+ к сере и к кислороду, а также от стойкости сульфата к термической диссоциации.
Сульфаты свинца и кадмия, характеризующиеся высокой стойкостью к диссоциации и меньшим сродством Me2+ к кислороду, чем к сере, восстанавливаются до сульфидов. Например:
PbSO4 + 4 СО = PbS + 4 СО2 , (12.3)
а основной сульфат свинца восстанавливается по реакции
РbО - PbSO4 + 5 СО = Pb + PbS + 5 СО2 . (12.4)
При достаточно низких температурах, при которых сульфаты цинка термически стойкие, восстановление протекает по реакциям
ZnSO4 + 4CO = ZnS +4C02;
ZnO • 2ZnSO4 +8 СО= ZnO + 2 ZnS + 8 СО2 .
Сульфат меди термически менее стоек, чем сульфаты свинца, кадмия, цинка, а СuО - легко восстановимый оксид, поэтому CuSO4 восстанавливается до металла:
CuSO4 + 2 СО = Сu + 8Ог + 2 СО2 . (12.7)
Таким образом, химизм восстановления сульфатов определяется соотношением скоростей термической диссоциации и восстановления. Если диссоциация протекает быстрее, чем восстановление, то конечный твердый продукт процесса — трудновосстановимый оксид или металл. Если быстрей протекает восстановление сульфата, то конечным продуктом процесса будет сульфид металла. Повышение температуры неодинаково ускоряет термическую диссоциацию и восстановление сульфата, и это может изменить химизм процесса: например, при низких температурах образуется сульфид, а при более высоких температурах - металл.
В цинковых агломератах содержится силикат цинка, который в условиях, характерных для восстановления агломерата, достаточно полно восстанавливается с образованием паров металлического цинка, а высвободившийся кремнезем связывается с породообразующими оксидами в силикаты.
При углетермическом восстановлении цинка из различных окисленных материалов он возгоняется в форме металла, тогда как другие возгоняемые компоненты имеют различные летучие формы, в которых они преимущественно отгоняются: свинец в виде PbS; кадмий в виде металла и CdS; индий в виде 1nС13 и InO; хлор в виде ряда хлоридов, но основной из них А1С13.
Вельцевание цинковых кеков, цинковистых шлаков и других материалов
Сущность и назначение велъцевания
В отечественной практике цинкового производства вельцевание — наиболее распространенный пирометаллургический процесс восстановления цинка.
Сущность процесса состоит в том, что цинксодержащий дисперсный материал смешивают с коксиком и при максимальной температуре, исключающей плавление материала, перемешивают шихту для равномерной газификации коксика и отгонки цинка по всей массе шихты. Такой процесс углетермического восстановления протекает интенсивно благодаря сильно развитой межфазной поверхности взаимодействующих веществ и тесному контакту восстановителя с восстанавливаемыми фазами при участии активного СО в момент его образования, а также благодаря отводу продуктов реакций из зоны протекания процессов восстановления.
Сохранение до конца процесса восстанавливаемого материала в твердом состоянии исключает растворение остаточных цинксодержащих фаз в общей массе материала. Поэтому вельцевание позволяет достичь низких остаточных концентраций цинка в переработанном материале.
Дисперсность твердого восстановителя (коксик) и твердых восстанавливаемых материалов исключает значительное возрастание внутридиффузионных сопротивлений процессу. Благодаря этому достигаются при достаточно больших скоростях восстановления низкие остаточные концентрации цинка в шихте.
При вельцевании возгоны окисляются в непосредственной близости от поверхности шихты. Поэтому затраты на эндотермические реакции восстановления в значительной мере компенсируются тепловыделением при окислительных реакциях. Непрерывное перемешивание шихты и противоток газа и шихты во вращающйся печи обеспечивают хороший теплоотъем шихтой от футеровки печи и от газового слоя вблизи шихты, который разогрет за счет сгорания возгонов. Благодаря этому вельц-процесс требует сравнительно небольшого удельного расхода коксика как топлива, главным образом на компенсацию теплопотерь с отходящими газами и через стенки вельц-печи.
Вследствие перечисленных особенностей процесса вельцевание эффективно для переработки твердых дисперсных и небогатых по цинку промпродуктов цинкового, свинцового и других производств, перерабатывающих цинксодержащее сырье, а также промпродуктов обогащения и богатых окисленных цинковых и медно-цинковых руд. Процесс не ограничивает влажность исходных шихт. Они не требует высокой квалификации обслуживающего персонала благодаря устойчивости режима.
Наиболее распространено вальцевание цинковых кеков и гранулированных цинковистых шлаков.
Практика вельцевания
Для осуществления процесса используют вельц-печь — трубчатую вращающуюся вокруг своей оси печь, имеющую небольшой угол наклона к горизонту для создания направленного перемещения шихты от верхнего загрузочного торца к нижнему торцу, через который выгружают твердый остаток перерабатываемой шихты. Этот остаток называют клинкером. Схематически вельц-печь показана на рис. 116.
С нижнего торца печи вдувают воздух, который подогревают факельной горелкой в период пуска печи для быстрого подъема температуры в печи или для восполнения теплолритока от горения коксика. При правильно подобранном режиме процесса подтопка горелкой не нужна, но горелка облегчает управление процессом и ей обычно пользуются. Клинкер высыпается из печи в яму с водой, где происходит его охлаждение и грануляция. Газовый поток в печи направлен от нижнего торца к верхнему и создается напорным вентилятором на нижнем конце и отсасывающим вентилятором на верхнем конце), сасывающий вентилятор подключают за пылеуловителями).
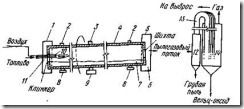
Рис. 116. Схема вельц-печи с комплектующими узлами:
1 — нижняя головка печи; 2 - опорные бандажи; 3 — венечная шестерня на привод; 4 - корпус печи; 5 - верхняя головка печи; 6 — загрузочный торец печи; 7 — слой шихты; 8 - опорные ролики; 9 - привод; 10 - короткофакельная горелка (на мазуте или природном газе); 11 - выпускной торец печи; 12 - пылевая камера; 13 -кулера; 14 - рукавные фильтры
Пылегазовый поток по выходе из печи попадает в пылевую камеру, где оседает грубая пыль (механический унос шихты), через кулера (батарея труб, через стенки которых газ охлаждается наружным воздухом), а затем через рукавные фильтры, где улавливаются возгоны (вельц-оксид). Грубую пыль из пылевой камеры возвращают в оборот (в шихту вельцевания), а вельц-оксид обычно направляют на выщелачивание.
Для нормальной работы вельц-печи необходимо в шихте создавать восстановительную газовую среду, а в газовом потоке над шихтой - окислительную. Кислород в дутье расходуется на газификацию восстановителя, на сжигание коксика как топлива и на окисление возгонов. При полном использовании газообразного кислорода, попадающего в шихту, в газовом потоке не должно быть СО, а содержание СО2 и О2 в потоке связано с объемной и линейной скоростями подаваемого в печь воздуха, а также с температурой газового потока и шихты в печи.
Так как возгоны содержат компоненты с разной способностью к окислению (Znпар окисляется значительно легче, чем PbS, Cd, CdS), то для полноты окисления возгонов, что повышает их качество, приходится повышать ![]() в отходящих газах путем подачи подсосом "вторичного" воздуха на выходе газов из печи. Для интенсификации горения коксика и возгонов, а также для повышения
в отходящих газах путем подачи подсосом "вторичного" воздуха на выходе газов из печи. Для интенсификации горения коксика и возгонов, а также для повышения ![]() в отходящих газах может быть использовано обогащение "первичного' воздуха кислородом.
в отходящих газах может быть использовано обогащение "первичного' воздуха кислородом.
Влияние состава шихты на процессы и превращения в шихте
Оптимальный режим вельцевания и показатели процесса зависят от химического, фазового и гранулометрического состава шихты. Эти условия имеют важное значение для процесса.
Шихта для вельцевания состоит из цинксодержащего окисленного материала и коксика. Содержащийся в шихте коксик служит топливом, восстановителем и "осушителем" — веществом, впитывающим расплавленную часть шихты. Поэтому количество коксика в шихте больше необходимого для сгорания, и в клинкере содержится "осушающая" часть коксика. Для понижения температуры воспламенения топлива часть коксика (20—30 %) заменяют углем той же крупности — штыбом. Крупность коксика должна быть оптимальной. Мелкие фракции интенсивно горят и выносятся с пылегазовым потоком. Это излишне повышает температуру реакционной массы (оплавляется масса и снижается отгонка металлов), а также ухудшается качество возгонов (повышается их восстановительная способность). Крупный коксик недостаточно активен из-за ограниченной удельной поверхности.
В вельцуемом материале, который мельче коксика, должно быть ограничено содержание основных отгоняемых металлов (Zn, Pb) и их соотношение. Верхний предел содержания цинка и свинца обусловлен временем пребывания материала в печи.
Если в материале много свинца (цинковые кеки, пыль свинцового производства и др.), то его шихтуют с другим материалом, в котором содержимся достаточно цинка, но мало свинца (цинковистые шлаки, песковая фракция цинкового огарка после кислого выщелачивания).
Если вельцуют только цинковые кеки, то расход коксика по отношению к подсушенным кекам (~20 % Н20) составляет 35—50%, крупность коксика 3—6 мм, максимальная температура реакционной массы 1350°С, содержание углерода в клинкере 15—20 %. Если вельцуют только цинковистые шлаки, то расход кокса по отношению к шлакам 45—55 %, крупность коксика до 15 мм, максимальная температура реакционной массы 1100-1200°С. Различия в условиях вельцевания названных материалов обусловлены различием плавкости исходных и образующихся материалов. Важно, чтобы в процессе вельцевания материалы не оплавлялись в значительной степени, в противном случае прекращаются восстановительные реакции в шихте, так как легкий коксик всплывает в более плотном расплаве, т.е. расслаиваются восстановитель и окисленный материал. Поэтому стараются при вельцевании поддерживать шихту "сухой". Однако если велыгуемый материал содержит значительное количество кремнезема (15-20 % SiO2), то повышается образование шлакового расплава и процесс ведут при "полужидком" состоянии шихты: твердая шихта пересыпается, но обильно смочена расплавом. Однако такой режим вельцевания менее производителен.
Одной из причин повышения плавкости реакционной массы является понижение tпл и вязкости цинковистых шлаков вследствие обеднения их по ZnO. Отрицательное влияние этого эффекта на вельцевание уменьшается при добавках в шихту СаО для восполнения удаляемого ZnO.
По характеру процессов, протекающих на различных участках печи, ее можно разделить на следующие зоны: 1) подготовительную, 2) возгоночную и 3) формирования клинкера. В подготовительной зоне в результате теплообмена между газом и шихтой последняя разогревается, из нее удаляется влага, сульфаты частично разлагаются до оксидов (степень десульфуризации достигает 35-50 %) и восстанавливаются до сульфидов, свободная Fe2O3 восстанавливается до Fel-xO, а связанная в ZnO(Fe, Mn)2О3 восстанавливается до (Zn, Fe)0·(Fe, Mn)2O3. Вероятно, в этой зоне коагель кремниевой кислоты, содержащийся в цинковом кеке, взаимодействует с сульфатами цинка и свинца, связывая их в силикатное стекло с частичной десульфуризацией. В зоне формирования клинкера идет догорание коксика и завершаются твердофазные процессы.
Наиболее важные превращения происходят в возгоночной зоне, где участки интенсивной возгонки кадмия, цинка и свинца не совпадают и следуют по ходу шихты в порядке перечисления (рис. 118) в соответствии с нарастанием температуры и кинетикой отгонки их летучих форм: Cd0, Zn0, CdS, PbS.

Рис. 118. Степень возгонки металлов
1 - свинец; 2 — цинк; 3 - кадмий
Возгоночную зону можно расширить введением "вторичного" воздуха в печь, повышением ![]() в дутье добавками технического кислорода, введением в шихту смеси коксика с углем (последний имеет более низкую tнач горения), подсушиванием кеков (сокращает L1). Расширение возгоночной зоны позволяет повысить производительность вельц-печи, или степень отгонки металлов, или верхний предел содержания цинка в вельцуемом материале.
в дутье добавками технического кислорода, введением в шихту смеси коксика с углем (последний имеет более низкую tнач горения), подсушиванием кеков (сокращает L1). Расширение возгоночной зоны позволяет повысить производительность вельц-печи, или степень отгонки металлов, или верхний предел содержания цинка в вельцуемом материале.
Удельную производительность вельц-печей Q выражают или массой переработанной шихты, или массой цинка и свинца в полученных возгонах, отнесенной к 1 м3 внутреннего объема печи в сутки. Производительность по возгонам (возгоночная .способность) QB более характеристична, чем производительность по шихте Qш, так как при прочих равных условиях QB меньше зависит от содержания Zn и РЬ в шихте и в какой-то степени связана с извлечением металлов в возгоны.

Рис. 119. Возгоночная способность вельц-печи θВ, т.е. количество отогнанных цинка и свинца на 1 м3 внутреннего
объема печи в сутки, в зависимости от соотношения Zn/Pb (по массе) в цинковом кеке
При благоприятном составе шихты (мало Рb и Сu) для печей с L = 41 м QВ =0,15÷0,2 т/(м3-сут), но при повышении относительного содержания Рb в шихте, т.е. при уменьшении Zn: Pb от 15 до 5, снижается QВ до 0,125, а далее QВ падает еще резче (рис. 119). Производительность печи прямо пропорциональна доле длины возгоночной зоны к общей длине печи, отношению Zn/Pb в шихте, распределенной температуре в возгоночной зоне.
Вельцевание раймовки по условиям и показателям аналогично вельцеванию цинковых кеков. Поведение окисленных цинковых руд при вельцевании может несколько отличаться от поведения кека из-за большей основности образующихся шлаковых расплавов, что приводит к большей плавкости шихт и интенсивному росту железистых настылей. При отмеченных особенностях руд их вельцевание улучшается при подшихтовке цинковистыми шлаками.
Настылеобразование
Главной причиной нарушения процесса вельцевания является образование настылей, снижающих производительность печи и нарушающих нормальное движение шихты в ней. Обобщая сведения, накопленные при изучении настылей, можно заключить следующее.
Настыли в печах размывают путем увеличения содержания коксика в шихте, что позволяет существенно повысить температуру реакционной массы в печи.
Продукты велъцевания
Продуктами вельцевания материалов являются вельц-оксид - промежуточный продукт (перерабатывается гидрометаллургически в цинковом производстве; грубая пыль — оборотный продукт (возвращается на вальцевание); клинкер, который при достаточном содержании меди является полупродуктом (перерабатывается в медном производстве) , а в противном случае является отвальным продуктом и хранится в отвалах предприятия (содержит благородные металлы, свинец и цинк).
Дистилляция цинка из агломерата
Углетермическое восстановление цинка и отгонка его из агломерата по существу те же, что и при рассмотренном выше процессе вельцевания, но процесс конденсаций иной. Необходимо сразу получать из возгонов металлический цинк. Для этого процесс возгонки и конденсации требует высоких рс„ в газовой фазе. При умеренных расходах углерода надо ограничиться малыми количествами воздуха при осуществлении дистилляции цинка, что является главной особенностью дистилляции цинка из агломерата. Техническое осуществление такого процесса сопряжено со значительными трудностями. Поиск способов, уменьшающих эти трудности в производстве, привел к разработке целого ряда аппаратов, каждый из которых имеет свои достоинства и недостатки.
Дистилляция цинка в горизонтальных ретортах. Реторты этого типа представляют собой цилиндр овального сечения длиной 1,8-1,9 м и диаметрами 340-370 и 230-260 мм с толщиной стенок и дна 30-40 мм, изготовленных из огнеупорной глины, шамота и коксика. Эти реторты в количестве 200-1000 шт. устанавливаются в специальной печи, отапливаемой газом. Топочные газы омывают и разогревают реторты снаружи. Реторты наклонены под небольшим углом вниз открытым концом, который присоединен герметично к индивидуальному конденсатору. Конденсаторы изготовлены из огнеупорной глины с измельченным ретортным боем. Внутренние стенки конденсатора глазурированы для лучшего отделения конденсата. Конденсатор представляет собой коническую трубу длиной 0,5-0,9 м, которая широким концом присоединена к реторте, а узким — к стальному сосуду (алонжу). Алонж - это сужающаяся труба, у которой широкий конец соответствует размеру горловины конденсатора, а узкий конец имеет отверстие 0,1 м, через которое выходит отходящий и дожигаемый газ, содержащий СО.
В каждую реторту загружают до 100 кг шихты, которая состоит из агломерата и оборотных продуктов (пыль из конденсатора и продукт переработки конденсаторного лома), а также угля (до 40 % в шихте). Уголь должен содержать мало золы, летучих веществ и серы, чтобы не вызвать сплавления шихты и сульфидирования цинка, так как ZnS - нелетучая форма. Крупность угля и агломерата должны быть 3—6 мм, что обеспечивает газопроницаемость шихты.
Дистилляция в горизонтальных ретортах - периодический процесс с суточной цикличностью.
Основной объём работы по обслуживанию печи выполняется в утренней смене ("маневр печи") и занимает 4-5 ч. В период маневра из конденсаторов выгребают последние порции цинка, разнимают конденсатор и реторту, очищают конденсатор, выгружают из реторты раймовку (остаток от дистилляции цинка из шихты), загружают в реторту свежую порцию шихты, устанавливают на место конденсатор и алонж, примазывая их для плотности глиной. Затем в течение суток поддерживают температурный режим печи, 3—4 раза выгребают из конденсаторов цинк и удаляют из алонжей пусьеру (пылевидные возгоны). Эту операцию выполняют после разъема алонжа и конденсатора, выгребают возгоны через горловину конденсатора и широкий торец алонжа. Все обслуживание печей ручное и связано с тяжелым трудом. Описанная технология обеспечивается ретортами и конденсаторами собственного производства, которое весьма трудоемко. Реторты должны быть достаточно прочными и жаростойкими. Срок службы шамотных реторт 36-40 сут, кампания печей 3-5 лет.
Дистилляция в горизонтальных ретортах ведется при температуре шихты 1200-1250°С. Наружные печные газы имеют температуру 1300-1350°С.
Печи с горизонтальными ретортами имеют низкий тепловой к.п.д. (~20 %) и высокое удельное потребление угля (~ 3 т на 1 т Zn). Общее извлечение цинка (с учетом оборотных продуктов) составляет в лучшем случае 89-92 % при прямом выходе цинка 70-75 % и следующем примерном распределении цинка по продуктам, %: черновой цинк 82,8; раймовка 6,3; пусьера 4,8; глина от подмазки конденсаторов 4,8; обломки конденсаторов 1,1; потери с газами 1,1; обломки реторт 0,7. Минимальный расход на 1 т цинка реторт 2-2,5 и конденсаторов 6-10. Выход раймовки составляет 30 % от загруженного агломерата и в ней содержится до 14 % Zn, из которых половина цинка окисленного, а остальное в виде ZnS.
Дистилляция цинка в горизонтальных ретортах имеет ряд недостатков: периодичность; низкое извлечение цинка и плохое его качество; низкие удельная производительность и тепловой к.п.д. печей; невозможность их механизированного обслуживания; трудо- и материалоемкость сопряженного производства керамических реторт и конденсаторов (соизмеримо с производством цинка). Этот способ наиболее старый, отмирающий.
Дистилляция цинка в вертикальных ретортах является непрерывным процессом, в котором утилизируется тепло топочных и отходящих технологических газов. Это выгодно отличает вертикальные реторты от горизонтальных. Вертикальная реторта - это шахта высотой 10-12 м, прямоугольного сечения шириной 300-330 мм и длиной 1,5-2 м, толщина стенок 40-250 мм (рис. 120). Стенки реторты выложены из карборундового кирпича на карборундовом цементе. К длинным сторонам реторты примыкают камеры сгорания, которые отапливаются природным или генераторным газом, а также отходящим газом из реторты рСО. В топочных камерах t = 1300÷1350°C. Малая толщина реторты (300 мм) ограничена теплопроводностью шихты, в которой г = 1275÷1300°С.

Рис. 120. Вертикальной -реторта:
I - реторта; 2 - камера сгорания газа; 3 - загрузочное устройство; 4 - разгрузочное устройство;
5 - конденсатор; 6 - верхний уровень шихты; 7 - скруббер; 8 -отстойник
Возгоночная зона в реторте имеет высоту 8 м, а над ней располагается еще слой свежей шихты в необогреваемой части реторты высотой
Столь высокий слой шихты требует специальной ее подготовки (см. ниже), обеспечивающей прочность и проницаемость шихты для газа.
Шихту периодически (через 1-1,5 ч) загружают в реторту сверху через устройство с механическими затворами и выпускают внизу через необогреваемое разгрузочное устройство с гидравлическим затвором. Таким образом, загрузка и выгрузка шихты не нарушают герметичность реторты. В реторте противоточно движутся шихта вниз, а газ вверх [последнее достигается дутьем снизу с небольшим расходом воздуха (0,2 м3/мин)].
Парогазовая смесь при 950-1000°С из верхней части реторты отводится в обогреваемый конденсатор, в котором поддерживается температура 560°С и благоприятные условия для конденсации путем разбрызгивания жидкого цинка из конденсата в газовом объеме конденсатора. Из конденсатора газы при 450-470°С отводятся в скруббер (орошаемый водой пылеуловитель), где улавливается пусьера, которая содержит до 62 % Zn и является оборотным продуктом, возвращаемым в шихту агломерации, а технологический газ из скруббера возвращается в камеры сгорания, отапливающие реторту.
Конденсированный цинк содержит 99,8 % Zn, 0,15 % Pb , 0,04 % Cd и не требует дополнительного рафинирования. Раймовка в виде брикетов, выгруженных из реторты через гидрозатвор, имеет влажность около 50 %, а,в сухом виде содержит, %: С 51, Fe2O3 .19,5, Zn 5,72, Pb, 1,37, Си 0,8, S 0,4, SiO, 9,5, А12ОЭ 5,0, CaO 2,6, MgO 1,26, Mn3O4 0,2, Ag 192 г/т. Этот полупродукт хранят в отвалах (он способен самовозгораться и загрязнять атмосферу).
Однако и вертикальные реторты имеют ряд серьезных недостатков: низкая производительность, сложная подготовка агломерата к дистилляции цинка, необходимость специального хранения брикетированной раймовки.
Электротермическая дистилляция цинка основана на использовании электроэнергии для нагрева шихты и применяется в двух вариантах: 1) переработка высококачественного (с низким содержанием примесей) агломерата без расплавления шихты в шахтных электропечах; 2) переработка низкокачественного (низкое содержание Zn и высокое содержание Fe и Си) агломерата с расплавлением в руднотермических электропечах. В шахтной электропечи восстановление и дистилляцию цинка ведут из твердой шихты, содержащей агломерат и кокс, а нагревают шихту электрическим током, проходящим через шихту, которая служит телом сопротивления.
Шахтная электропечь, схематически представленная на рис. 121, имеет высоту 11-14 м, диаметр 1,75-2,4 м. В печи на двух разных уровнях по высоте размещены по диаметру восемь электродов (расстояние между уровнями 7,3-9,7 м). Шихта, заполняющая печь, служит телом сопротивления. Электроды изолированы от корпуса печи.
Высококачественные агломераты, состав и способ получения которых рассмотрены ранее, дробят и классифицируют по крупности на куски разных размеров от 5 до 20 мм и в определенном соотношении фракций. Такой агломерат шихтуют с равным количеством более крупного кокса и грузят в шахтную электропечь. Содержание кокса в шихте в три раза превосходит теоретически необходимое для восстановления цинка, что позволяет сохранить примерное постоянство электрического сопротивления столба шихты по высоте, несмотря на частичное выгорание кокса. Шихту предварительно разогревают во вращающейся барабанной печи и с помощью специального вращающегося загрузочного устройства распределяют крупные фракции шихты по центру печи, а более мелкие - по периферии.
Такое распределение шихты создает распределение температуры по горизонтальному сечению шихты с максимумом по центру (1300-1400°С) и минимумом у стенок (900-950°С). Столб шихты опирается на медленно вращающийся разгрузочный стол. Между корпусом печи и этим столом имеется зазор, через который выгружают раймовку. Скорость вращения разгрузочного стола и величину зазора регулируют и таким образом изменяют скорость продвижения шихты по печи сверху вниз.
Через центр разгрузочного стола в печь подают дутье с малым расходом воздуха. Газ поднимается через столб шихты вверх до расширяющейся зоны печи, которая расположена на 1/3 межэлектродного расстояния от верхнего ряда электродов. В расширяющейся части печи расположен кольцевой желоб с нижней прорезью, по которому собирается газ с возгонами и направляется в конденсатор. Конденсатор - вакуумного типа с водяным охлаждением через стенки. Степень конденсации цинка 92-94 %. Отходящий газ, содержащий 80 % СО, 1,6 % СО2, 15 % N2; 1,5 % О2, очищают в скруббере, за которым стоит вакуумный насос.
Срок службы таких печей невелик (~ 100 сут), а их ремонт весьма трудоемок. Высокие требования к химической чистоте и физическим свойствам агломерата, большой расход электроэнергии (2500-2900 кВт-ч/1т Zn) оправдывают этот процесс при прямом получении цинка высокого качества. Прямой выход цинка 78-85 %, общее извлечение цинка90 %, содержание цинка в раймовке 15 %. Раймовку охлаждают и классифицируют по крупности: фракцию крупнее 19 мм направляют в отвал (она бедна по цинку), средняя фракция (она богата коксом) является оборотной и возвращается в шихту, а мелкая фракция после отделения из нее магнитной фракции тоже оборотная и возвращается в шихту (она богата по цинку).
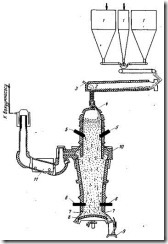
Рис. 121. Шахтная электропечь:
1 - бункеры с агломераторм; 2 - прокалочная печь; 3 - горелка; 4 - питатель; 5 -верхние электроды; 6 - нижние электроды; 7 - водоохлаждаемый опорных обод; 8 - вращающийся разгрузочный стол; 9 - ковшовый транспортер; 10 - кольцевой газосборник; 11 — конденсатор
В руднотермической электропечи восстановление и дистилляцию основной части цинка осуществляют из твердой шихты, состоящей из агломерата и кокса, и лишь малую долю цинка, переходящего в жидкий шлак, восстанавливают расплавленным медистым чугуном, который выплавляется из шихты. Электрический обогрев шихты и плавление шлакообразующих осуществляют пропусканием тока через жидкий шлак как тело сопротивления.
Руднотермическая печь (рис. 122) имеет прямоугольную форму. Корпус печи стальной, футерован высокосортным глиноземистым кирпичом. Подина -воздухоохлаждаемая, а стенки - водоохлаждаемые. Электрообогрев печи осуществляют пропусканием тока через шлаковый расплав. Ток подводят тремя графитовыми электродами, которые или погружены в шлак, или замыкаются на него открытой электрической дугой. Электроды могут вертикально перемещаться, таким образом изменяют силу тока и температуру в печи.
Для переработки в руднотермической печи пригодны шихты любой влажности, нет жестких ограничений на гранулометрический состав и со держание цинка в агломерате (20-60 % Zn), приемлемы высокозольные (до 20 % золы) со значительным содержанием летучих (до 6 %) угли, в которых, однако, не менее 60 % свободного углерода.
Рис. 122. Руднотермическая электропечь:
1 - печь; 2 - контейнер; 3 - электроды; 4 - питающий электрический трансформатор; 5 — конденсатор; б - зумпфы для жидких продуктов; 7 - летки
Во избежание таких осложнений можно повысить содержание серы в шихте и получить вместо чугуна штейн с меньшей tпл. При этом допустимо повышение СFe в шлаке.
Особенностью переработки цинкового агломерата в руднотермических печах является то, что в шихту вводят только стехиометрически необходимое количество восстановителя (кокса) для восстановления отгоняемых металлов (Zn, Pb, Cd) и для частичного восстановления железа. Степень восстановления железа выбирают такой, чтобы его содержание в шлаке превышало 1,5 %, так как при меньшем его содержании восстанавливаются кремний, магний, кальций, пары которых неблагоприятны для 246 конденсации цинка. Во всех ранее рассмотренных агрегатах, напротив, восстановитель задается со значительным избытком. Эта особенность обусловлена тем, что из руднотермической печи материал выгружается только в виде пара и жидких продуктов (шлак и чугун или штейн), а кокс не выводится и ограниченно газифицируется из-за отсутствия дутья. Поэтому избыток кокса будет накапливаться в печи, что нарушит материальный баланс в агрегате. Отсутствие избытка восстановителя приводит к меньшему р„„ в отходящих газах, несущих пары цинка. Это повышает долю оксида цинка в конденсате. Поэтому при руднотермической дистилляции цинка его конденсация требует специфических условий. Недостаток СО в газовой фазе компенсируется повышенной температурой ее на выходе из печи (~ 1000°С), при которой СO2 еще не окисляет Zn , а принудительно охлаждаемый и разбрызгиваемый в конденсаторе жидкий цинк позволяет быстро охлаждать и конденсировать парообразный цинк (см. §3).
В агломерате для руднотермической электроплавки необходимо иметь соотношение СаО : Si02 = (0,8-1,4): 1, что дает достаточно жидкотекучий шлак при 1350°С, не вызывающий осложнений при его выпуске из печи.
Шихту перед загрузкой в печь в течение 2 ч разогревают и прокаливают при 850—900°С в трубчатой вращающейся печи. При этом отгоняется влага, разлагаются карбонаты, частично восстанавливается Fe2O3 до FeO, отгоняются летучие из кокса. Прокалочную печь отапливают технологическим газом от электропечи, содержащим СО, Горячую шихту выгружают в теплоизолированный бункер и оттуда специальными контейнерами периодически (через 1 ч) загружают по 2-3 т в электропечь через воронки в ее своде, расположенные вдоль стен печи. Шихта образует откосы вдоль стен печи. Уровень откосов шихты, глубина шлакового, а под I ним чугунного расплава контролируются. Толщина шлакового и чугунного слоев должны быть достаточными для периодического выпуска значительных количеств этих продуктов без риска замыкания электрической дуги на подину и короткого замыкания через чугун. Температуру расплава поддерживают на уровне 1450°С. Защитой стенок от воздействия столь высокой температуры служат шихтовые откосы. Температура жидкого цинка в конденсаторе равна 500°С.
Руднотермическая электроплавка требует большего удельного расхода электроэнергии на 1 т цинка и дает более грязный цинк, чем шахтная электроплавка, но имеет преимущества в более низких требованиях к сырью, в подготовке шихты, в степени и комплексности извлечения металлов, проще в эксплуатации, требует менее дорогие огнеупоры.
Дистилляция цинка в шахтных печах отличается от прочих способов получения цинка из агломерата тем, что ведется на воздушном дутье, следствием чего является значительное количество технологических газов с низким содержанием цинка и значительным содержанием СO2 - Это требует других условий конденсации металлического цинка. Иными средствами достигается высокая прочность крупного агломерата, необходимого для шахтной печи.
Особенность шахтной цинковой плавки состоит в необходимости выдерживать жесткие технологические условия по составу отходящего газа, по температуре в печи и в конденсаторе.
Сущность процесса состоит в том, что крупный и достаточно прочный агломерат [прочность достигается добавками в шихту агломерации свинцовых или свинцово-цинковых материалов так, чтобы в шихте отношение Zn:Pb=(2-3):1]; вместе с крупным коксом (без значительного избытка) пропускается через шахтную печь, работающую на воздушном дутье. В печи происходит углетермическое восстановление цинка частично из твердых фаз и частично из расплава. Цинк и часть свинца отгоняются и с отходящими газами поступают в конденсатор, орошаемый жидким свинцом. Из нижней части печи выпускают шлак и металлический свинец (не-возогнанная часть). Процесс разработан под руководством Моргана (S.W.К. Morgan) и промышленно осуществлен английской фирмой "Imperial Smelting Co" и назван IS-процессом. Этот процесс осуществляют в шахтной печи прямоугольного сечения. Стенки печи кессонированы, а в верхней части футерованы шамотным кирпичом (рис. 123). Длинные кессонированные стенки создают сужение печи книзу и через них введен двухярусный ряд фурм в узкую зону печи, что обеспечивает равномерное распределение воздушного дутья по центральной части сечения печи. Торцевые стенки вертикальны по всей высоте. Через боковые стенки выше уровня шихты печь сообщается с конденсаторами. Колошник печи закрытого типа. Шихту загружают через два колокольных затвора), и обеспечивают герметичность газового тракта), расположенных по длинной оси сечения.
Особенностью этого процесса является необходимость высокой температуры на верхнем уровне шихты, чтобы исключить окисление и преждевременную конденсацию металлического цинка (см. § 3).
Шахтные печи для IS-процесса имеют площадь сечения в области фурм 7-12,6 м2, высота зоны реакции 5,1-5,5 м, количество фурм 18-30 шт., производительность единичных агрегатов по шихте 100-300 т/сут.
Конденсаторы (один или два на печь) — прямоугольные камеры, футерованные карборундовым кирпичом в них имеются мешалки для разбрызгивания жидкого свинца, который циркулирует между конденсатором и ликвационной камерой, где поглощенный в конденсаторе цинк выделяется из свинца. Газы из конденсатора поступают в скруббер (мокрый пылеуловитель), который улавливает в виде пусьеры несконденсировавшуюся часть возгонов, и затем газы выбрасываются в атмосферу. Жидкие продукты плавки выпускают из печи в отстойную камеру, где расслаиваются и отдельно выпускаются шлак, штейн и черновой свинец.
IS-процесс ведут в непрерывном режиме. Загрузка шихты периодическая. Шихта состоит из агломерата и кокса одинаковой крупности (60-90 мм). Для поддержания высокой температуры на верхнем уровне шихты без увеличения количества технологических газов в печь загружают кокс, подогретый до 800°С. Агломерат готовят из цинкового концентрата, свинецсодержащего материала (руда, концентрат, полупродукт) и оборотных материалов так, чтобы в нем соотнощение по массе Zn:Pb = 1,8÷3,0 (снижение этого отношения вызывает настылеобразование в печи, а повышение снижает прочность агломерата).

Рис. 123. Шахтная печь для lS-процесса:
1 - циклон-брызгоуловитель; 2 - скруббер; 3 - водяные форсунки; 4- конденсатор; 5 - роторные мешалки; 6 - загрузочное устройство; 7 — насос для перекачки свинца; 8 - сифон для выпуска свинца; 9 - приемник для цинка; 10 - ликвационная ванна; 11 -корпус шахтной печи; 22 - горн печи; 13 — фурмы; 14 - отстойник для разделения шлака и чернового свинца; 15 - воздухонагреватель; 16 - вентилятор
Примерный состав агломерата, %: Zn 35-40; Pb 15-20; Si02 7-8; СаО 9-10; S< 1.
В печь подают подогретое до 600°С воздушное дутье не только через фурмы, но и в область над верхним уровнем шихты (12 % от общего объема дутья) для создания в отходящих из печи газах достаточно высокой (~ 1000°С) температуры, чтобы исключить окисление возгонов. В фокусе печи t ≈ 1400°С, чтобы исключить образование тугоплавкого чугуна (см. § 3). Расход кокса составляет 90 % от массы возгоняемого цинка (на свинец тепло не расходуется) плюс 20 % от массы образующегося шлака.
Принцип действия конденсатора основан на том, что свинец ограниченно растворяет цинк, растворимость растет с повышением температуры. Свинец в конденсаторе имеет температуру 560°С и содержит 2,4 % Zn; в ликвационной камере от охлаждается до 450°С, что вызывает выделение растворенного в нем цинка в верхнем жидком слое. Этот слой выпускают, а охлажденный свинец, содержащий 2 % Zn, вновь возвращается в конденсатор. Кампания печи длится от 4 мес до 1 года.
Состав чернового цинка, %: Zn 98,5-98,8; Pb 1,1-1,3; Cd 0,03-0,15; Сu 0,01-0,05; Sn 0,005-0,015; Fe 0,015-0,028; Ag 0,001-0,008; As 0,01-0,04. Состав чернового свинца, %: Pb 98,5-99; Zn 0,02-0,05; Cu 0,2-0,6; Sn 0,001-0,03; As 0,01-0,04; Sb 0,15-0,50; Bi 0,01-0,03; 430-460 Ag/т. Состав шлака, %: СаО 30-32; Si02 20-25; FeO 20-32; A1203 6-11;Zn 6-7; Pb 0,5-0,8; Cu 0,5. В черновой цинк выходит 91-93 % Zn, а в черновой свинец - до 89 % Pb. Черновые металлы подвергают рафинированию.
Оборотными материалами являются пусьера и дроссы (пыль, осевшая в конденсаторе, и продукты окисления цинка). В оборотные продукты переходит до 15 % от общего количества цинка в шихте.
Удельная производительность печи, т/(м2·сут): по шихте 12-32, по цинку 5-13, по свинцу 2,5-6. Площадь сечения печи в области фурм 17-27 м2.
Достоинства IS-процесса следующие: высокая производительность печей и их механизация; умеренный расход топлива; возможность комплексно перерабатывать разнообразное и сложное по составу сырье (коллективные концентраты, сульфидные руды, промпродукты обогащения и металлургического производства). К недостаткам процесса относятся высокие требования к качеству агломерата, низкое качество цинка, необходимость высококвалифицированного обслуживания.
Сырье для производства меди и никеля. вспомогательные материалы
В зависимости от вида присутствующих минералов руды цветных металлов классифицируются на 4 типа:
1) сульфидные, в которых металлы присутствуют в форме сульфидов (медные, медно-никелевые и другие полиметаллические руды);
2) окисленные, в которых металлы находятся в форме кислородсодержащих соединений — оксидов, гидроксидов, карбонатов и т. д. (никелевые и медные руды);
3) смешанные, в которых металлы могут находиться как в сульфидной, так и в окисленной форме (медные руды);
4) самородные, содержащие металлы в свободном состоянии (медные руды). В самородном состоянии в природе встречаются также золото, серебро и платина.
Сульфидные руды по типу оруднения делятся на сплошные и вкрапленные (порфировые). Как следует из самого названия, в сплошных рудах основную массу составляют сульфиды, содержание же в них компонентов пустой породы (SiO2, СаО, Аl2Оз и др.) незначительно (10—20%). Во вкрапленных рудах картина обратная — основную массу руды составляет пустая порода, а содержание сульфидов в них невелико.
По числу присутствующих в рудах металлов их классифицируют на монометаллические и полиметаллические (комплексные). Большинство руд цветных металлов являются полиметаллическими и содержат до 10 и более ценных компонентов. Наиболее сложными по составу являются медно-цинковые, медно-свинцово-цинковые, медно-никелевые, медно-молибденовые, медно-кобальтовые руды. Включая в название ведущий ценный спутник, определяют тем самым тип руды со всем комплексом ценных составляющих.
Руды меди и никеля, как правило, очень бедные и содержат всего несколько процентов, а часто и доли процентов основного металла. Концентрация в них ценных элементов-спутников обычно еще меньше. Однако многие сопутствующие элементы по ценности даже превосходят основные компоненты руды. Важнейшими ценными спутниками меди в рудах являются золото, серебро, селен, теллур, цинк, свинец, кадмий, таллий, висмут, сурьма, молибден, рений и др., включая серу сульфидных руд. Одновременное присутствие в рудах всех перечисленных ценных элементов не является обязательным. Они присутствуют в разных сочетаниях, свойственных данному типу руды или месторождения.
Характерными спутниками никеля в медно-никелевых рудах являются кобальт, платина, палладий, золото, серебро, осмий, иридий, родий, рутений и некоторые другие элементы.
При оценке рудного сырья необходимо также учитывать характер присутствующей пустой породы. По этому признаку руды подразделяют на кислые и основные. В кислых рудах пустая порода в основном представлена кремнеземом; при пирометаллургической переработке эти руды требуют добавки основного флюса — известняка. Основные руды, наоборот, требуют кислых, кремнистых флюсов.
Кларк меди, т. е. ее содержание в земной коре, равен 0,01%. Однако, несмотря на низкое содержание в земной коре, она образует многочисленные месторождения руд — естественные скопления рудных медных минералов. Характерным для меди является наличие в природе руд всех четырех рассмотренных выше типов.
Известно более 250 медных минералов. Большинство из них встречаются сравнительно редко, некоторые представляют собой драгоценные камни. К наиболее распространенным медным минералам, имеющим промышленное значение при получении меди, относятся прежде всего соединения меди с серой и кислородом. Наибольшее количество меди в земной коре (около 80%) входит в состав сернистых соединений. Ниже приведены важнейшие сульфидные минералы меди:
Минерал Си, %
Ковеллин CuS 66,5
Халькозин Cu2S 79,9
Халькопирит CuFeS2 34,6
Борнит Cu5FeS4 63,3
Кубанит CuFe2S3 23,5
Талнахит* CuFeS(i,e-2) 36—34,6
Кроме того, довольно распространены медно-мышьяковистые (энаргит Cu3AsS4) и медно-сурьмянистые (тетраэдрит Cu3SbS3) минералы.
Сульфидные медные минералы имеют как гидротермальное, так и магматическое происхождение. При высоких температурах и давлениях вода, выделяющаяся при застывании магмы, наряду с сульфидами меди растворяет сульфиды, селениды и теллуриды многих других металлов и прежде всего железа, цинка, свинца, мышьяка и сурьмы. В растворе содержатся также благородные металлы, висмут и редкие металлы. При охлаждении термальных вод из них выкристаллизовывается целый комплекс ценных минералов: халькопирит CuFeS2, сфалерит ZnS, галенит PbS.
Основными компонентами пустой породы являются пирит FeS2 и кварц. Соотношение между ценными минералами может „меняться в широких пределах. Совместная кристаллизация минералов, особенно если она протекала сравнительно быстро, часто приводит к очень-тонкому их прорастанию, что крайне затрудняет разделение ценных минералов при обогащении. Поскольку температура кристаллизации различных минералов неодинакова, состав, руды меняется по глубине месторождения. Меняются также стехиометрический состав однотипных минералов и содержание в них примесей.
Магматические месторождения, содержащие медь, образуются при кристаллизации ультраосновных пород. В этих месторождениях важнейшими спутниками меди являются никель, кобальт, платиновые металлы. Железо кристаллизуется в виде пирротина FeS,никель в основном в виде пентландита (Fe, Ni)S, но частично он может входить изоморфно и в состав пирротинов. Таким образом, и в магматических месторождениях медь встречается в комплексе со многими другими ценными элементами.
В природных условиях первичные сульфидные минералы могут подвергаться воздействию атмосферных агентов (кислорода, СОг, воды) и претерпевать изменения (выветриваться). Очень часто ковеллин и халькозин являются продуктом превращения первичных минералов. Более глубокое превращение приводит к образованию кислородных соединений меди.
Старейшей рудной провинцией является Урал. По восточному склону Уральского хребта с севера на юг полосой протяженностью около 800 км разбросана большая группа медных месторождений, приуроченных к так называемым зелено-каменным породам. К этой группе относятся месторождения Турьинской группы, районов Кировграда, Красноуральска, Среднеуральска, Медногорска, Гая, Сибая, Карабаша.
Руды восточного склона Уральского хребта относятся к категории медно-цинковых сульфидных руд. Основными спутниками меди в них являются цинк, свинец, золото, серебро, часто присутствуют висмут, германий, кадмий, индий, таллий, селен, теллур. Руды подвергают селективному обогащению с получением медного, цинкового и пиритного концентратов. Они являются основной сырьевой базой для медных заводов и комбинатов Урала: Красноуральского, Среднеуральского, Карабашского и Медногорского.
На западном склоне Уральского хребта в так называемых пермских песчаниках расположёны многочисленные, но небольшие по мощности месторождения преимущественно окисленных медных руд. Некоторые из этих месторождений были базой медной промышленности в XVII—XVIII вв. В настоящее время их практически не используют. В целом Урал, занимавший когда-то ведущее положение в производстве меди, свое главенствующее положение утратил. Запасы уральских медных руд постепенно истощаются. Центр тяжести в производстве меди перемещается в Казахстан и Заполярье.
Важными источниками медного сырья в Казахстане являются Коунрадское, Саякское и Джезказганское месторождения. Они обеспечивают рудой Балхашский и Джезказганский горно-металлургические комбинаты. Руды данных месторождений относятся к категории вкрапленных. Основной вмещающей породой этих руд является кварц, т. е. они относятся к кислым породам. Ценными спутниками меди во вкрапленных рудах являются молибден и рений. Содержание благородных металлов невелико.
Отличительной особенностью казахстанских месторождений являются их большая мощность и залегание вблизи земной поверхности. Поэтому разработку месторождений ведут открытым способом с использованием мощной современной техники, что обусловливает относительно низкую стоимость руды.
Вкрапленные руды легко обогащаются, а полученные при этом концентраты характеризуются высоким содержанием меди (так, джезказганские концентраты содержат до 40% меди). Большие масштабы производства, применение дешевых методов добычи руды и хорошая их обогатимость позволяют вовлекать в эксплуатацию руду с содержанием 0,3% меди. Кроме Джезказганского и Коунрадского месторождений, в Казахстане имеется еще несколько крупных месторождений такого же типа, например Бощекульское.
Наряду с вкрапленными рудами в восточном Казахстане имеются месторождения пиритных медно-цинковых руд, близких по составу к уральским (Орловское, Николаевское, Белоусовское и др.). В Казахстане имеется также большое количество (около 1000) мелких месторождений окисленных руд, которые пока не вовлекают в эксплуатацию.
Крупнейшим центром производства меди за последнее время стало Заполярье. Сырьем этого района являются медно-никелевые руды Кольского полуострова и уникальные месторождения района Норильска (полуостров Таймыр). Ценными спутниками меди в рудах этого типа являются никель, кобальт, сера, селен, теллур, металлы платиновой группы, золото и серебро, причем на долю платиновых приходится значительная часть общей стоимости ценных компонентов руды. Медно-никелевые руды в основном магматического происхождения; встречаются как сплошные сульфидные, так и вкрапленные руды. Содержание пустой породы в сплошных рудах составляет всего 15%, остальное — сульфиды.
Основными медными минералами являются халькопирит, кубанит и талнахит, а основным сопутствующим минералом — пирротин. Никель встречается преимущественно в виде пентландита (Ni, Fe) S. Некоторое количество никеля находится также в виде твердого раствора в пирротинах. Высокое содержание в рудах этого района благородных металлов, меди, никеля и кобальта делает их переработку экономически очень выгодной, несмотря на удаленность региона и тяжелые климатические условия Заполярья. В ближайшие десятилетия основные капиталовложения и основное увеличение производства меди и никеля ожидаются именно в этом районе.
Медные руды добывают также в Средней Азии (район Алмалыка) и в Закавказье (Армения), где имеется ряд месторождений сульфидных пиритных руд. Уникальное месторождение вкрапленных медных руд (Удоканское) разведано в Забайкалье.
Вследствие низкого содержания медилексного характера медных руд в большинстве случаев их непосредственная металлургическая переработка невыгодна, поэтому их предварительно подвергают, как правило, селективному флотационному обогащению. При обогащении медных руд основным продуктом являются медные концентраты, содержащие до 55% меди (чаще от 10 до 30%). Извлечение меди в концентраты при флотации колеблется от 80 до 95%. Кроме медных, при обогащении руд часто получают пиритные концентраты и концентраты ряда других цветных металлов (цинковый, молибденовый и т. д.). Отходами обогащения являются отвальные хвосты.
Флотационные концентраты представляют собой тонкие порошки с частицами крупностью менее 74 мкм и влажностью 8—10%.
В металлургии меди и никеля роль предварительного обогащения очень велика. От содержания ценного компонента в перерабатываемом сырье зависят производительность металлургических агрегатов, расход топлива, электроэнергии и вспомогательных материалов, трудовые затраты, потери извлекаемых компонентов и в конечном итоге себестоимость готовой продукции.
Предварительное обогащение рудного сырья, значительно более дешевое, чем непосредственная металлургическая переработка, обеспечивает:
- снижение затрат на последующие металлургические операции и себестоимости конечного продукта в первую очередь за счет сокращения объема перерабатываемых материалов;
- возможность переработки бедных руд, непригодных для прямой металлургической переработки, т. е. расширение запасов природного сырья;
- в ряде случаев повышение комплексности использования исходного сырья за счет выделения ценных компонентов в отдельные концентраты, пригодные для дальнейшей самостоятельной металлургической переработки.
Медные руды и получаемые при их обогащении концентраты имеют одинаковый минералогический состав и отличаются лишь количественными соотношениями между различными минералами.
Следовательно, физико-химические основы их металлургической переработки будут совершенно одинаковы.
Значительные осложнения возникают при обогащении сложных по составу, труднообогатимых полиметаллических руд, например уральских медно-цинковых руд. При их селективном обогащении, кроме медного, цинкового и пиритного концентратов, в значительном количестве получается так называемый промпродукт, содержащий часто 8—10% меди и до 16—18% цинка. Он резко снижает извлечение меди и цинка в одноименные концентраты и создает огромные трудности в его металлургической переработке. Переработка промпродукта традиционными металлургическими методами даже с удовлетворительными технико-экономическими показателями фактически невозможна. Если же при обогащении идти по пути сокращения выхода промпродукта или полностью предотвратить его получение, это резко ухудшит качество основных концентратов, что отрицательно повлияет на работу металлургических переделов. Для переработки сложных по составу промпродуктов в настоящее время разрабатывают новые технологические процессы.
Основным сырьем для получения никеля являются окисленные никелевые и сульфидные медно-никелевые руды. В небольших количествах за рубежом его получают из мышьяковистых руд.
В России доля никеля, получаемого из сульфидных медно-никелевых руд, по сравнению с окисленными никелевыми рудами непрерывно возрастает. За рубежом наблюдается обратная тенденция.
Окисленные (силикатные) никелевые руды являются рудами вторичного происхождения. Они образовались в результате выветривания главным образом змеевиков и состоят из простых и сложных гидратированных силикатов магния и железа и алюмосиликатов, содержащих никель.
Окисленные никелевые руды содержат незначительное количество никеля — от десятых долей до 1,5—3%. Только в некоторых рудах содержится до 5% и более никеля. В основном эти руды состоят из пустой породы. В рудах обязательно содержится кобальт. Отношение никеля к кобальту в них составляет (25—40): 1. В значительных количествах (до 0,02%) в рудах может присутствовать медь, практически во всех случаях руды содержат хром (до 1—2% и более).
Основными никельсодержащими минералами в окисленных рудах являются гарниерит (Ni, Mg) О- SiO2 • 2Н2О, ревдинскит и непуит 3(Ni, Mg)O*2SiO2*2Н2О и нонтронит nNiO • (Al, Fe)2O3X X4SiO2 • 4Н2О. Никелевые минералы в рудах находятся в тонко-диспергированном состоянии. Пустую породу составляют серпентин 3MgO • 2SiO2 • 2Н2О, каолинит А12О3 • 2SiO2 • 2Н2О, тальк 3MgO • 4SiO2 • 4Н2О, кварц и некоторые другие минералы. Железо в таких рудах находится в форме оксидов и гидроксидов, в которых присутствует никель.
По соотношению между содержаниями важнейших компонентов окисленные никелевые руды классифицируют на несколько промышленных типов, среди которых можно выделить следующие основные виды: железистые (более 30% Ре2Оз), железисто-кремниевые (менее 30% Fе2Оз), железисто-магнезиальные (6—11% MgO), магнезиальные (до 20% MgO) и кремнистые (до 50% SiO2).
Силикатные руды отличаются высоким содержанием влаги — в среднем 20—25%, а иногда до 40%. Характерной особенностью этих руд являются также их высокая неоднородность и исключительное непостоянство химического состава по содержанию как никеля, так и пустой породы. Колебания состава наблюдаются даже в массиве одного месторождения. Возможные пределы концентраций компонентов руды следующие, %: 0,5—5,0 Ni; 0,04—0,16 Со; 15-50 SiO2; 15-65 Fe2O3; 2-25 MgO; 5-16 А12О3; 0,5-2 CaO.
По внешнему виду окисленные никелевые руды похожи на глину. Для них характерны пористое, рыхлое строение, малая механическая прочность кусков, высокая гигроскопичность, рассеянность никеля почти по всем минералам и тесное прорастание одних минералов в другие. Такое физико-химическое состояние окисленных никелевых руд делает невозможным механическое вскрытие индивидуальных минералов, содержащих никель, и следовательно, их отделение от пустой породы при обогащении традиционными методами.
Среди возможных путей обогащения окисленных никелевых руд следует назвать метод, сочетающий их предварительное пирометаллургическое сульфидирование в трубчатых вращающихся печах с последующим флотационным выделением образовавшихся сульфидов из измельченного спека. Такой способ прошел проверку в производственных условиях и показал положительные результаты. Однако промышленного применения он не нашел.
Из-за отсутствия рациональных методов обогащения окисленные никелевые руды в настоящее время поступают непосредственно в металлургическую переработку.
В Советском Союзе промышленные месторождения окисленных никелевых руд расположены на Урале, в Казахстане и на Украине, а за рубежом — в Новой Каледонии, на Кубе, в США, Бразилии и Греции.
Сульфидные медно-никелевые руды частично уже были рассмотрены в предыдущем разделе. В сульфидных рудах никель присутствует главным образом в виде пентландита, представляющего собой изоморфную смесь сульфидов никеля и железа переменного соотношения, и частично в форме твердого раствора в пирротине. Значительно реже в природе встречается чистый никелевый сульфид — миллерит NiS. Из других природных сульфидов можно отметить очень редкие минералы — полидимит и природный ферроникель.
Основным спутником никеля в сульфидных рудах является медь, содержащаяся главным образом в халькопирите, кубаните и талнахите. С учетом высокого содержания меди в этих рудах их и называют медно-никелевыми. Кроме никеля и меди, в медно-никелевых рудах обязательно присутствуют кобальт (до 3% от содержания никеля), а также металлы платиновой группы (платина, палладий, родий, рутений, осмий и иридий), золото, серебро, селен и теллур. Таким образом, сульфидные медно-никелевые руды являются полиметаллическим сырьем очень сложного химического состава. При их металлургической переработке извлекают 14 (включая серу) ценных компонентов.
По структуре медно-никелевые руды могут быть сплошными, жильными и вкрапленными. Чаще встречаются два последних типа руд. В зависимости от глубины залегания рудных тел их добывают как открытым, так и подземным способом.
В отличие от окисленных никелевых руд сульфидные медно-никелевые руды характеризуются высокой механической прочностью, негигроскопичны. Основную часть медно-никелевых руд подвергают предварительному обогащению.
В России месторождения сульфидных медно-никелевых руд находятся в северных районах страны — на Таймырском и Кольском полуостровах. За рубежом запасы медно-никелевых руд сосредоточены в Канаде и Австралии.
Основным способом обогащения сульфидных медно-никелевых руд является флотация. Иногда флотационному обогащению предшествует магнитная сепарация, направленная на выделение пирротина в самостоятельный концентрат. Возможность проведения магнитной сепарации обусловлена относительно высокой магнитной восприимчивостью пирротина. Получение пирротинового концентрата, содержащего до 1,5% никеля, не всегда оправдано, так как возникает необходимость в организации его специальной переработки с целью извлечения никеля, серы и платиноидов.
Флотационное обогащение может быть коллективным или селективным. При коллективной флотации ставится задача отделить пустую породу и получить обогащенный продукт — медно-никелевый концентрат. Селективная флотация позволяет не только освободиться от пустой породы, но и выделить большую часть никеля и меди в самостоятельные концентраты. Полного разделения меди и никеля при селективной флотации провести не удается, и второй продукт селекции по существу является медно-никелевым концентратом, отличающимся от руды значительно более высоким отношением Ni/Си. На практике такой концентрат обычно называют просто никелевым.
Таким образом, при обогащении сульфидных медно-никелевых руд в зависимости от принятой схемы обогащения могут получаться коллективные медно-никелевые, медные, никелевые и пирротиновые концентраты.
Медные концентраты с высоким соотношением меди и никеля, равным примерно 20:1, перерабатывают на медеплавильных заводах.
Кроме окисленных никелевых и сульфидных медно-никелевых руд, сырьем для получения никеля могут служить мышьяковистые руды, которые представлены типичными жильными образованиями. В этих рудах арсениды никеля тесно ассоциированы с арсенидами кобальта, сульфидами меди и других металлов. Наибольшие запасы мышьяковистых руд имеются в Марокко, Иране, Франции, Канаде и Бирме. Вследствие ограниченности запасов мышьяковистые руды не имеют большого значения в производстве никеля.
Электроплавка окисленных никелевых руд
Основным способом переработки окисленных никелевых руд являлась их плавка в шахтных печах на штейн. Однако этот способ сопряжен с высоким расходом кокса и флюсов и характеризуется низким извлечением никеля и кобальта в штейн. Рост потребности в легированных никелем сталях явился стимулом для применения других более простых и высокоэффективных процессов переработки окисленных никелевых руд. К таким процессам, получающим в последние годы все большее развитие, относится восстановительная электроплавка руд на ферроникель. Получение ферроникеля в электропечах обеспечивает высокое извлечение никеля, кобальта и железа из руды и значительно упрощает технологию ее переработки по сравнению с плавкой в шахтных печах на штейн.
При плавке на ферроникель в электропечах перерабатывают агломерированную или предварительно прокаленную в трубчатых печах руду. Иногда процесс прокалки руды совмещают с ее предварительным восстановлением. Прокалка, обеспечивающая удаление гигроскопической и конституционной влаги, а также частичное восстановление руды способствуют значительному снижению расхода электроэнергии при последующей электроплавке. В зарубежных странах при электроплавке окисленных никелевых руд в основном стремятся извлечь никель, в связи с чем плавку ведут на богатый ферроникель. В отличие от зарубежной практики в России при плавке получают бедный ферроникель, что обеспечивает наряду с извлечением никеля высокое извлечение кобальта, а также более полное извлечение железа из руды.
В процессе восстановительной электроплавки окисленных никелевых руд, кроме никеля, кобальта и железа, в сплав переходят также некоторые количества углерода, кремния, хрома, фосфора и серы. Поэтому для получения кондиционного ферроникеля требуется проведение дополнительных операций для удаления указанных примесей.
Поведение компонентов шихты при восстановительной электроплавке на ферроникель
Железо, никель, кобальт. При восстановительной электроплавке окисленные соединения железа, никеля и кобальта, восстанавливаясь, переходят в сплав. Чем больше восстановителя в шихте, тем больше восстанавливается железа и тем беднее по содержанию никеля и кобальта будет получаемый сплав, но зато тем выше будет их извлечение из руды в этот сплав.
Следует отметить, что скорости плавления шихты, восстановления железа и взаимодействия его с силикатным расплавом при заданной мощности печи зависят еще от целого ряда факторов, среди которых решающее значение имеют составы исходной шихты и образующихся в результате плавки сплава и шлака. Отсутствие в настоящее время данных об активностях компонентов сплава не позволяет пока рассчитывать оптимальные составы шлака и сплава, обеспечивающие минимальные потери никеля со шлаками. Однако совершенно очевидно, что получение при плавке сплава с минимальным содержанием кремния может обеспечить максимальное извлечение никеля в сплав.
Кремний. Хотя SiO2 восстанавливается значительно труднее, чем окислы железа, никеля и кобальта, все же благодаря высокой его концентрации в шихте при электроплавке окисленных никелевых руд образуется некоторое количество кремния, часть которого реагирует с окислами железа, никеля и кобальта, восстанавливая их до металлов, образующих сплав, а часть растворяется в образующемся сплаве.
Восстановление кремнезема окисью углерода по реакции
SiO2 + 2CO=Si + 2C02 (5)
маловероятно с точки зрения термодинамики, так как даже при температуре 1727°С кремний окисляется до SiO2 газовой фазой, содержащей тысячные доли процента углекислого газа.
В присутствии железа, являющегося растворителем кремния, равновесие реакции восстановления SiO2 твердым углеродом смещается вправо.
Восстановление SiO2 в условиях избытка углерода возможно также с образованием карбида кремния:
SiO2 + 3C = SiC + 2CO. (9)
Однако в присутствии железа процесс предпочтительнее идет с образованием кремния, растворенного в жидком железе.
При восстановительной плавке окисленных никелевых руд имеет место окисление кремния закисью железа шлака:
Si + 2FeO=SiO2 + 2Fe
Данные полупромышленных и промышленных плавок окисленных руд на ферроникель показывают, что равновесное распределение кремния между продуктами плавки достигается только при шлаках, содержащих менее 50% (мол.) SiO2 и 17% (мол.) MgO или не более 55% SiO2 (мол.) при высоком содержании в них MgO (25—30% мол.). Дальнейшее увеличение содержания кремнезема в шлаках приводит к повышенному (против равновесного) переходу кремния в сплав. С уменьшением основности шлаков, когда сокращается число свободных ионов кислорода и структура кремнекислородных анионов заметно усложняется, массоперенос кислорода в жидких шлаках резко уменьшается, а следовательно, и уменьшается скорость окисления кремния, что способствует его повышенному переходу в сплав.
Учитывая отмеченные особенности поведения кремния при восстановительной электроплавке, необходимо для получения чистого по кремнию ферроникеля регулировать состав отвального шлака путем шихтовки разных типов руд и загрузки в печь флюсов. Кроме того, необходимо менять количество восстановителя при изменении состава руд.
Углерод. Поведение углерода при электроплавке окисленных никелевых руд определяется составом сплава и расходом восстановителя. При увеличении расхода восстановителя увеличивается содержание кремния в сплаве, что приводит к снижению растворимости в нем углерода. Кремний и никель снижают растворимость углерода в железе, хром оказывает обратное действие.
Хром. В процессе электроплавки окисленных никелевых руд присутствующая в исходной шихте окись хрома восстанавливается по реакции
Cr2О3 + 3C = 2Cr + 3CO, (11)
начиная с температуры примерно 1100° С. Переход хрома в сплав в значительной степени определяется извлечением в него железа: чем выше извлечение железа, тем выше переход Сг в сплав.
Сера и фосфор. Сера в процессе электроплавки вводится исходной рудой и восстановителем, фосфор — в основном рудой. В случае предварительного обжига руды 28% серы переходит в газы и пыль. При электроплавке примерно 26% серы переходит в сплав, 24,5% — в шлак и около 50% — в газы; 50% фосфора переходит в сплав и 50% — в газы.
Электроплавка сульфидных медно-никелевых руд и концентратов
Электроплавка сульфидных медно-никелевых руд и концентратов получила широкое распространение в металлургии никеля. Электропечи применяют на всех медно-никелевых предприятиях. На отечественных предприятиях электроплавке подвергают руды и агломерированные или гранулированные, прокаленные на агломерационной ленте медно-никелевые концентраты. На заводах в электропечах перерабатывают обожженные в печи кипящего слоя концентраты в смеси с кварцевым флюсом. Кроме твердой шихты, в электропечах перерабатывают жидкий конвертерный шлак, однако доля этого оборотного материала в шихте рудной электроплавки на отдельных предприятиях различна и зависит главным образом от характера исходной твердой шихты и наличия на заводе печей для отдельной переработки конвертерных шлаков. Для получения бедных по содержанию никеля и кобальта шлаков в шихту электроплавки вводят небольшие количества восстановителя — коксовой или угольной мелочи.
Первоначально отечественные предприятия вели бесфлюсовую плавку тугоплавких руд и концентратов с повышенным содержанием в них окиси магния и кремнезема и пониженным содержанием железа.
Конструкция рудно-термических печей, применяемых для переработки сульфидных медно-никелевых руд и концентратов, аналогична конструкции печей медной плавки. На медно-никелевых заводах в настоящее время применяют электропечи с площадью пода от 58 до 184 м2 и мощностью установленных на них трансформаторов 18 000—50 000 кВА. Большинство печей оборудовано гидравлической системой перепуска и перемещения электродов. Шлаковый пояс электропечей отечественных заводов охлаждается заложенными в футеровку медными холодильниками, а подина — воздухом, нагнетаемым по каналам, проложенным между бетонной подушкой и футеровкой.
Содержание меди, никеля, и кобальта в шлаках. Важным вопросом электроплавки медно-никелевых руд и концентратов является снижение потерь меди, никеля и кобальта с отвальными шлаками. Многочисленные исследования, проведенные на отечественных заводах, дали возможность установить факторы, влияющие на содержание этих металлов в электропечных шлаках. В частности, подтвердилось, что с повышением содержания FeO в шлаке он становится богаче медью, никелем и кобальтом. Также подтвердилось, что конвертерные шлаки обедняются до состава отвальных только в случае, если их заливают в электропечь в небольшом количестве (примерно до 10% от массы твердой шихты). При заливке больших количеств конвертерного шлака увеличивается содержание FeO в печном шлаке и потери меди, никеля и кобальта с ним возрастают.
Содержание цветных металлов в штейне в значительной степени влияет на их содержание в отвальном шлаке и, кроме того, металлизированные (содержащие свободное железо) штейны обладают способностью обеднять богатые (в том числе и конвертерные) шлаки, в особенности по кобальту. Это объясняется тем, что равновесие в системе
Fe + MeO ↔FeO + Me (2)
сдвинуто вправо в большей степени, чем в системе
FeS + MeO ↔FeO + MeS. (3)
В процессе работы на металлизированных штейнах было установлено, что при температуре штейнов 1200—1250°С предельное содержание в них металлического железа не должно превышать 20%, в противном случае избыток железа будет выпадать из расплава и образовывать настыли, затрудняющие нормальный выпуск штейна из электропечи.
Согласно исследованиям А. В. Ванюкова, увеличение отношения Сu : Ni в штейне оказывает влияние на увеличение механических потерь цветных металлов со шлаками вследствие снижения величины межфазного натяжения. Вместе с ростом содержания меди в штейнах несколько снижается степень их металлизации, что также приводит к увеличению потерь металлов со шлаками. Для повышения межфазного натяжения необходимо увеличение содержания SiO2 в электропечных шлаках.
Конвертирование никелевых и медно-никелевых штейнов
Термодинамика основных реакций процесса
Никелевые штейны, являющиеся продуктом восстановительно-сульфидирующей плавки окисленных никелевых руд, по своим свойствам существенно отличаются от медных и медно-никелевых штейнов. Никелевые штейны не расслаиваются на сульфидную и металлическую фазы и при любом содержании серы могут при соответствующей температуре находиться в виде однородной жидкости.
Результаты минералогического и химического анализов застывших штейнов шахтной плавки окисленных никелевых руд показывают, что основными их составляющими являются сульфидная фаза, а также твердый раствор железа, никеля и кобальта. Содержание металлической фазы в штейне может достигать 30—40%. В ней присутствует около 40—60% Ni; 60—70% Со и 30—40% Fe от общего содержания этих металлов в штейне. В никелевых штейнах находится около 2—3% магнетита, с которым ассоциирована небольшая часть кобальта (~10%). Остальные металлы образуют сульфидную фазу. Присутствие металлической фазы в никелевых штейнах отражается на особенностях процесса конвертирования и на его тепловом режиме.
Медно-никелевые штейны по фазовому составу отличаются от никелевых повышенным содержанием дополнительной сульфидной составляющей Cu2S и металлической меди. Количество магнетита в этих штейнах зависит от способа плавки исходного сырья. В штейнах электроплавки при наличии углерода в шихте его мало. Электропечные штейны могут содержать 10—20% металлической фазы.
При подаче дутья в штейновую ванну конвертера с кислородом прежде всего будут взаимодействовать металлы по схеме 2 Me + О2 = 2 МеО.
Очевидно, в первую очередь будет окисляться металлическое железо с образованием FeO и Fe304. Вслед за железом может происходить окисление кобальта, а затем никеля. Однако образующиеся СоО и NiO при определенных условиях передают часть кислорода неокислившемуся металлическому железу:
(СоО) + [Fe] ↔ (FeO) + [Со], (15)
(NiO) + [Fe] ↔ (FeO) + [Ni]. (16)
Кроме того, NiO и СоО могут реагировать с FeS штейна:
3 (NiO) + 3 [FeS] + O2 = [Ni3S2] + 3 (FeO) + S02, (18)
(CoO)+ [FeS] == [CoS] + (FeO). (19)
Из-за отсутствия необходимых термодинамических данных для Ni3S2 Л. М. Шалыгин произвел оценку возможного хода взаимодействия закиси никеля с сульфидом железа применительно к упрощенной реакции
(NiO) + [FeS] = [NiS] + (FeO). (20)
Из экспериментальных данных следует, что пока в штейне присутствуют металлическое железо и FeS, степень окисления никеля и кобальта будет невелика. Тем более это справедливо для меди, поведение которой при конвертировании было рассмотрено ранее.
По мере снижения концентрации металлического железа при продувке штейна наступает равенство значений химических потенциалов или парциальных
молярных величин изменения энергии Гиббса реакций окисления FeS и металлического железа. В этих условиях термодинамически вероятно одновременное протекание обеих указанных реакций. Из сульфидов цветных металлов вначале должен окисляться сульфид кобальта и последним — сульфид меди. В реальных условиях заметное окисление кобальта начинается при содержании железа в сульфидном расплаве 12—13% .
Окислительным агентом при конвертировании является не только кислород дутья, но и сернистый газ. Исследования А. А. Вольского и В. И. Смирнова показали, что реакция
3FeS + 2S02 = Fe304+ 2,5S2 (21)
протекает с выделением элементарной серы. Элементарная сера в конвертере снова окисляется до S02.
Образование магнетита при конвертировании протекает как в результате взаимодействия закиси железа с кислородом дутья, так в результате реакции (21).
При рассмотрении процесса конвертирования никелевых штейнов большой интерес представляет взаимодействие сульфида никеля с закисью никеля:
[Ni3S2] + 4 (NiO) = 7 [Ni] + 2S02. (23)
Однако необходимо иметь в виду, что образующийся металлический никель растворяется в исходном сульфиде, в результате чего в системе возникает фаза переменного состава. При этом активность компонентой реакции (23) существенно изменяется.
Растворение металлического никеля в его сульфиде сдвигает равновесие реакции (23) в правую сторону и обусловливает, по-видимому, ее частичное протекание при обычных температурах конвертирования с получением металлизированного никелевого файнштейна.
При постоянном давлении рассматриваемая система является моновариантной и равновесный состав расплава однозначно определяется температурой. Расчет по уравнению (25), выполненный С. Е. Вайсбурдом, позволил получить зависимость остаточного содержания серы в расплаве от температуры при атмосферном давлении. Помимо расчета осуществлено экспериментальное определение температурной зависимости состава расплава. При достаточно высокой температуре (~1650° С) можно получать металлический никель с небольшим содержанием серы продувкой сульфидных расплавов. Результаты исследований показывают, что такая температура может быть достигнута при использовании кислородного дутья.
Конвертирование никелевых и медно-никелевых штейнов
В настоящее время на уральских заводах переработку штейнов осуществляют в горизонтальных конвертерах емкостью 20 и 30 т. На заводах Заполярья для конвертирования медно-никелевых штейнов применяют 40- и 80—100-т конвертеры. В качестве холодных материалов используют охлажденный штейн, электропечной шлак и обороты конвертерного передела, которые содержат не менее 5—10% Ni. В отдельных случаях в конвертерах перерабатывают отходы металлообрабатывающих заводов, содержащие от 10 до 40% Ni. Количество холодных присадок, вводимых в конвертер, зависит от состава штейнов и изменяется от 30 до 100% от массы жидкого штейна. Содержание SiO2 в кварцевых флюсах, применяемых при конвертировании медно-никелевых штейнов, составляет 70—75%; при конвертировании никелевых штейнов — не менее 85—90%.
Как известно, особенностью процесса конвертирования никелевых штейнов является наличие периода окисления металлического железа, в течение которого в конвертере развивается высокая температура. Расчеты показывают, что теоретическая температура в факеле может составлять 1650—1700° С. Практически в массе расплава она существенно ниже.
Изменение содержания железа и серы в штейне по ходу конвертирования, по данным В. А. Воробьева, В. Я. Зайцева и др., показано на графике (рис. 18). Из графика следует, что содержание металлического железа сравнительно быстро убывает по ходу процесса. Содержание серы в штейне сначала увеличивается с 19— 20 до 27—28%, держится на этом уровне пять — шесть продувок, а затем снижается к концу операции опять до 18—19%. До снижения содержания серы в продуваемом штейне его металлизация уменьшается, а затем растет, но уже за счет образования металлического никеля.
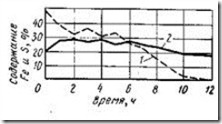
Рис. 18. Изменение содержания железа (1) и серы (2) в штейне по ходу конвертирования
При конвертировании никелевых штейнов из-за высокой температуры, развивающейся при выгорании металлического железа, холодные присадки обычно вводят сразу после заливки свежих порций штейна и подачи кварцевого флюса. В этот период необходимо стремиться к переработке максимального количества холодных присадок. Продувка продолжается 20—50 мин в зависимости от количества и состава поступивших материалов и количества подаваемого в конвертер воздуха. После слива первого шлака конвертер часто снова ставят на дутье и проводят одну или несколько «холостых» продувок с загрузкой кварцевого флюса и холодных присадок. По мере снижения содержания железа в сульфидной массе уменьшается ее объем и создаются более благоприятные условия для приема свежих порций штейна. «Холостые» продувки проходят не менее резким подъемом температуры, так как при этом окисляется сернистое, а не металлическое железо и на 1 кг вводимого кислорода выделяется меньше тепла. Из практики известно, что в период окисления металлического железа за каждую минуту дутья температура в конвертере повышается на 5—10°С, а в период окисления FeS за то же время — на 3°С.
Перед заливкой новых порций штейна богатая масса должна содержать не менее 20% Fe. Это необходимо для получения при конвертировании шлаков с низким содержанием никеля и кобальта, начинающих ошлаковываться по мере обогащения массы в конвертере. Значительный переход никеля и кобальта в шлак происходит при содержании железа в конвертерной массе соответственно менее 8 и 13% .
В практике конвертирования широко применяется работа с переливом, что позволяет увеличить извлечение никеля в файнштейн из-за меньшего выхода богатых конвертерных шлаков. Набор обычно осуществляют на нескольких конвертерах, доводку ведут в одном или двух, конвертерах. Обогащенная сульфидная масса, набранная для доводки файнштейна, содержит 64—74% Ni; 0,7-1,3% Со и 4-6% Fe.
Большое внимание при продувке штейнов уделяют извлечению кобальта в один из продуктов конвертирования. На уральских заводах кобальт стремятся максимально перевести в конвертерный шлак, на заводах Заполярья - оставить в файнштейне. Первый вариант обеспечивается наиболее полным удалением железа из сульфидного расплава (до 0,3%), второй - сохранением в нем некоторой части железа (2,5-3,5%). Для увеличения перевода кобальта в шлак на заводах, перерабатывающих никелевые штейны, проводят так называемое рафинирование файнштейна. Для этого в конвертер заливают свежую порцию штейна (1 -0,5 ковша) и осуществляют кратковременную продувку расплава воздухом (10-15 мин) с загрузкой кварца для .повышения температуры в конвертере и создания тем самым условий для перевода кобальта в шлак. После снижения содержания кобальта в массе до 0,5% приступают к окончательной доводке. Во избежание попадания в файнштейн шлаков при его сливе из конвертера последнюю продувку ведут с избытком кварцевого флюса для получения тугоплавких и вязких шлаков, которые при сливе файнштейна остаются в конвертере.
На заводах, перерабатывающих медно-никелевые штейны, перевод основного количества кобальта в файнштейн обеспечивают неполным удалением из него железа; повторным конвертированием штейнов, полученных при обеднении конвертерных шлаков; переработкой конвертерных шлаков периода доводки файнштейна, особо богатых по кобальту, в конвертерах, работающих во время набора; снижением температуры в конвертере в конце операции до минимальной (1180° С) за счет увеличенного расхода кварцевого флюса. Кроме того, период набора ведут при содержании железа в массе не менее 25%, что обеспечивает минимальный переход кобальта в конвертерный шлак, являющийся единственным полупродуктом, с которым кобальт выводится из процесса конвертирования.
Полученный медно-никелевый файнштейн разливают в специальные изложницы, причем от режима его охлаждения существенно зависят показатели последующего разделения меди и никеля флотацией. Разделительная флотация усложняется при образовании в файнштейне металлической фазы, поэтому снижение температуры в конце операции и неполное окисление железа необходимы также для предупреждения образования металлического никеля. По действующим техническим условиям содержание серы должно быть выше 20%, содержание железа не должно превышать 3,5%.
С целью повышения сортности металлического никеля Л. Л. Чермаком и др. разработан способ получения маложелезистого никелевого файнштейна. Способ основан на том, что с понижением температуры равновесие реакции (16) смещается в правую сторону и соответственно равновесная концентрация железа в файнштейне уменьшается. Жидкий файнштейн медленно охлаждают в открытом неотапливаемом отстойнике с 1250—1300 до 900° С, что на 100° С выше температуры затвердевания сульфидной составляющей файнштейна. Основная масса окислов выделяется в отстойнике, одновременно выкристаллизовывается часть металлической составляющей файнштейна. Эти полупродукты возвращают в оборот. Охлажденный файнштейн выпускают в песочные изложницы. Описанный способ позволяет снизить содержание железа в файнштейне в среднем до 0,24% и получить огневой никель преимущественно марки НЗ.
Вторым жидким продуктом конвертирования является конвертерный шлак. Исследования показали, что состав конвертерных шлаков по ходу процесса существенно меняется. При конвертировании никелевых штейнов содержание SiO2 в шлаках в начале и середине операции в среднем составляет 25—27%, к концу операции оно повышается до 30—32%, что объясняется необходимостью получения файнштейнов с минимальным содержанием железа. Одной из причин лучшего усвоения двуокиси кремния конвертерным шлаком является более высокая, температура по сравнению с конвертированием медных штейнов. Наибольшее содержание магнетита в конвертерных шлаках (18—22%) наблюдается в середине и конце операции конвертирования. В начале процесса, когда осуществляется продувка металлизированных штейнов, содержание магнетита в шлаках составляет 10—12%. Содержание SiO4 и Fe3O4 в конвертерных шлаках, образующихся при конвертировании медно-никелевых штейнов, не отличается существенно от содержания этих компонентов в шлаках медеплавильных заводов.
Содержание никеля и кобальта резко возрастает в шлаках последних сливов, что в свою очередь приводит к понижению концентрации FeS в сульфидном расплаве.
А. В. Ванюков и В. Я. Зайцев отмечают, что металлургические расплавы в процессе конвертирования находятся в состоянии, далеком от равновесия. Недостаточно высокие скорости процессов шлакообразования и восстановления магнетита сульфидами металлов по сравнению со скоростями реакций окисления сульфидов и образования Fe3O4 обусловливают повышенное сверх равновесного содержание в шлаках трехвалентного железа, а следовательно, и растворенных цветных металлов. При конвертирований никелевых и медно-никелевых штейнов содержание растворенных меди и никеля в шлаках периода набора составляет около 50- 70%, кобальта
Если переход меди и никеля в высокожелезистый шлаковый расплав в этот период происходит главным образом вследствие растворения их сульфидов при одновременном переходе в шлак катиона и аниона
[Me] - 2е ↔ (Ме2+),
[S] + 2e↔(S2-),
то растворение кобальта связано с развитием обменной реакции между компонентами штейновой и шлаковой фазы
[Со] + (Fe2+) 4↔ (Со2+) + [Fe].
Наличие в расплаве магнетита вызывает дополнительное растворение кобальта по реакции
3Fe3O4 + CoS ↔9FeO + CoO + SO2.
Так как на конвертирование поступают бедные штейны, то выход шлаков значителен, что отрицательно влияет на величину прямого извлечения никеля и меди в файнштейн. Для улучшения этого показателя при конвертировании никелевых и медно-никелевых штейнов применяют промывку шлака свежей порцией металлизированного штейна, которая может сопровождаться последующим отстаиванием расплавов в течение 3—5 мин. Этот прием позволяет снизить содержание цветных металлов в конвертерных шлаках за счет осаждения крупных штейновых включений, а также цементирующего действия металлического железа и восстановления им части магнетита конвертерного шлака, что приводит к росту межфазного натяжения на границе штейн — шлак. Конвертерные шлаки направляют на переработку для извлечения из них кобальта и других цветных металлов. При окислении металлической фазы никелевых штейнов образующиеся газы не содержат сернистого ангидрида. По мере выгорания металлического железа концентрация SO2 в них растет и к концу продувки достигает 10—13%, что близко к содержаниюSO2 в конвертерных газах медеплавильных заводов. Вместе с тем содержание серного ангидрида в газах, выделяющихся при конвертировании никелевых штейнов, значительно ниже содержания SO3 при конвертирований медных штейнов, поскольку более высокие температуры, развивающиеся при продувке никелевых штейнов, увеличивают степень термической диссоциации SO3.Так, содержание SO3 в отходящих газах конвертеров комбината «Южуралникель» составляет 0,02-0,03% (объемн.), тогда как при конвертировании медных штейнов концентрация S03 в газах достигает 1,0—1,5%.
Запыленность газов перед пылеулавливающими установками при продувке штейнов без добавки сыпучих материалов составляет примерно 1,25г/м3. При загрузке флюсов и других пылевидных материалов она возрастает до 75 г/м3. Абсолютная величина пылевыноса сравнительно невелика и колеблется в пределах 0,5—1,5% от массы перерабатываемого горячего штейна. Примерный состав конвертерной пыли на уральских заводах: 7— 25% Ni; 0,16-0,25% Сu; 0,3-0,7% Со; 13-40% Fe; 11-14% S; 18—22% SiO2, а на заводах Заполярья: 9—12% Ni; 10—15% Сu; 0,3-0,4% Со; 16-25% Fe; 10-12% S; 22-30% SiO2.
Переработка медно-никелевого файнштейна
Разделение медно-никелевого файнштепна флотацией
Режим охлаждения файнштейна. Медно-никелевый файнштейн имеет ясно выраженное кристаллическое строение и состоит из кристаллов двух видов: кристаллов сульфида никеля с небольшой примесью сульфида медики кристаллов сульфида меди с небольшой примесью сульфида никеля. В файнштейне с малым содержанием серы имеются кристаллы сплава меди с никелем. Структура медно-никелевого файнштейна показана на рис.78.
Исследованиями И. Н. Масляницкого и С. Л. Кричевского было установлено, что для разделения флотацией требуется медленное охлаждение файнштейна. В процессе охлаждения кристаллы каждого сульфида должны обособиться один от другого и вырасти до большого размера.

Рис. 78. Структура медно-никелевого файнштейна
Режим охлаждения файнштейна можно разделить на четыре периода. В течение первого периода масса файнштейна остается жидкой, и скорость охлаждения в этом периоде не имеет значения. Второй период начинается с появления первых кристаллов и включает все время кристаллообразования. Размеры кристаллов увеличиваются с уменьшением скорости охлаждения, поэтому для лучшего разделения файнштейна флотацией необходимо во время образования кристаллов охлаждать файнштейн медленно со скоростью не больше 28 град в час. Медленное охлаждение надо начинать с температуры на 60—100 град выше конечной температуры затвердевания файнштейна. Температура начала затвердевания файнштейна, содержащего 50—55% никеля и 20—25% меди, равна примерно 750—780°С, а файнштейна с соотношением Ni : Cu=l : 1 составляет 930° С, так как температура плавления у сульфида меди выше, чем у сульфида никеля. По окончании затвердевания в кристаллах сульфида никеля остается примерно до 2% сульфида меди. Третий период, является периодом превращения β-сульфида никеля в α-сульфид; превращение происходит в интервале температур 598—510°С. Превращение β-Ni3S2 в α-Ni3S2 сопровождается уменьшением концентрации Cu2S в твердом растворе сульфидов никеля. При медленном охлаждении файнштейна сульфид меди вытесняется из кристаллов сульфида никеля и отлагается на кристаллах сульфида меди, при этом кристаллы сульфида никеля Ni3S2 становятся более чистыми. На практике для лучшего обособления кристаллов сульфидов меди и никеля скорость охлаждения поддерживают в пределах 5 град в час. Соблюдение режима охлаждения в третьем периоде наиболее важно для обеспечения чистоты кристаллов сульфида никеля и сульфида меди в файнштейне.
Четвертым периодом охлаждения файнштейна является период после превращения β-Ni3S2 в α-Ni3S2. Теоретически этот период начинается при 510°С, но, учитывая время, требующееся для окончания превращения одной формы сульфида никеля в другую, медленное охлаждение надо продолжать до температуры, значительно более низкой (примерно до 100°С). Скорость охлаждения файнштейна в этом периоде может быть доведена до 50—60 град в час.
Чистота и степень разделения сульфидов никеля и меди определяются главным образом содержанием серы и железа в файнштейне. При повышении содержания железа ухудшается структура файнштейна и результаты его разделения, так как сульфиды меди и никеля загрязняются сульфидом железа. Исследования Северо-Кавказского горнометаллургического института показали, что при содержании в файнштейне 1—3% железа, охлаждать его следует со скоростью 10 град в час от 600—650 до 400—450° С. Выше и ниже этих температур охлаждение можно производить с большей скоростью.
Содержание серы определяет количество металлической фазы, которая является основным источником загрязнения концентратов, получаемых при флотации файнштейна, другим металлом, т. е. никелевого концентрата медью и медного концентрата никелем. Исследования показали, что при повышении содержания серы в файнштейне улучшается структура файнштейна и его разделение на никелевый и медный концентраты.
Флотация файнштейна. Перед флотацией блоки медно-никелевого файнштейна разбивают и дробят. Разбивку производят стальной бабой с электрокрана или копром. Дробление осуществляют в три стадии до 20 мм в щековых и конусных дробилках. В флотационном отделении файнштейн подвергают мокрому измельчению в две стадии в шаровых мельницах до размера частиц менее 0,04—0,05 мм с целью отделить кристаллики сульфидов один от другого. Отделению помогает то, что при дроблении куски файнштейна дают трещины преимущественно по местам соприкосновения разнородных кристаллов, а не по телу однородного вещества. Файнштейн с высоким содержанием серы хрупок и его дробление и измельчение не вызывает особых трудностей.
Схема флотации медно-никелевого файнштейна предусматривает получение двух конечных продуктов — никелевого и медного концентратов и третьего промежуточного продукта.
Флотацию файнштейна ведут в сильно щелочной среде с получением медного концентрата, всплывающего с пеной, и никелевого концентрата, не всплывающего с пеной. Для флотации применяют два реагента: соду каустическую (3—3,2 кг/т файнштейна), устанавливающую сильно щелочную среду, и ксантогенат калия (1 кг/т файнштейна), создающий условия для всплывания сульфида меди.
Пенный продукт (грубый медный концентрат) и непенный продукт многократно перечищают, в результате получают концентраты высокого качества: никелевый концентрат (68—70% Ni, 3—4% Сu) и медный концентрат (68—73% Сu и 3,5—5% Ni). В никелевый концентрат извлекается 96—97% никеля и около 92% кобальта и переходит около 8% меди, в медный концентрат — 91 — 92% меди и 3—4% никеля. Выход никелевого и медного концентратов зависит от состава файнштейна. Для некоторых файнштейнов выход никелевого концентрата составляет на одном заводе 55%, а на другом 67%, а медного соответственно 45 и 33%.
В отличие от флотационного обогащения руды при разделении медно-никелевого файнштейна флотацией отвальных хвостов не получают. Все металлы — никель, медь, кобальт и платиноиды распределяются между продуктами флотации и извлекаются при последующей переработке. Метод флотационного разделения медно-никелевого файнштейна экономически эффективен и получил широкое распространение.
Обжиг никелевого файнштейна и концентрата. Восстановительная электроплавка закиси никеля.
Теоретические основы окислительного и хлорирующего обжига
Процесс окислительного обжига никелевого файнштейна и концентрата от разделительной флотации сопряжен с известными трудностями, обусловленными спекаемостью материала при низких температурах. Поэтому до недавнего времени применяли двустадийный обжиг. Первую стадию обжига осуществляли в многоподовой печи с механическим перегребанием при умеренных температурах (400-800° С), вторую - в трубчатых вращающихся печах при повышенных температурах (800-1250° С). В настоящее время прогрессивный способ обжига применяют все никелевые заводы России и ряд зарубежных предприятий. При этом на медно-никелевых заводах, подвергающих обжигу никелевый концентрат разделительной флотации, вторая стадия обжига исключена на технологической схемы, а на заводах, перерабатывающих окисленные никелевые руды (в связи с необходимостью проведения промежуточной операции обезмеживания), обжиг файнштейна по-прежнему ведут в две стадии: сначала в печах кипящего слоя, а затем в трубчатых печах. В окислительной атмосфере обжиговой печи протекают реакции окисления составляющих файнштейна или концентрата. В первую очередь происходит окисление металлической составляющей
2Ni+O2 =2NiO
а затем окисление сульфида никеля:
Ni3S2 +3.5O2=3NiO+2SO2
При известных условиях в процессе обжига файнштейна и никелевого концентрата может иметь место образование сульфата никеля устойчивого при сравнительно высоких температурах. Сульфатообразование при обжиге облегчается тем обстоятельством, что закись никеля имеет каталитические свойства и способствует наиболее полному окислению сернистого ангидрида до серного.
Скорость процесса удаления серы из файнштейна увеличивается с повышением температуры, концентрации кислорода в дутье, а также с уменьшением крупности его частиц и степени металлизации. Хлорирующий обжиг является составной частью технологической схемы переработки никелевого файнштейна и предназначен для отделения от никеля небольших количеств меди. Последнее достигается переводом сульфидной и окисленной меди при обжиге в легко растворимые в воде хлориды. Хлорирующему обжигу подвергают никелевый огарок (продукт первой стадии окислительного обжига файнштейна), содержащий 1—3% S Процесс осуществляют в трубчатом вращающемся реакторе при начальной температуре 700—750° С за счет тепла горячего огарка (без отопления). В качестве хлорсодержащего реагента используют поваренную соль или сильвинит, добавляемые к огарку в количестве 10—12% от его массы.
Хлорид натрия разлагается сернистым или серным ангидридом печных газов в присутствии кислорода:
2NaCl + SO2 + O2 = Na2SO4 + C12,
2NaCl + SO2 + 1/2O2 = Na2SO4 + Cl2.
Скорость и полнота разложения поваренной соли увеличиваются с повышением концентрации окислов серы в газах и при наличии в шихте катализаторов (окислов железа и никеля). Выделяющийся при этом газообразный хлор очень активен и интенсивно хлорирует соединения металлов, присутствующих в огарке, в первую очередь соединения меди.
В основном никелевый огарок представлен окислами металлов (для успешного протекания процесса в нем должно содержаться не менее 1—2% S). Как показывают кинетические исследования, скорость хлорирования окислов меди, никеля, кобальта и железа при одинаковых температурных условиях различна. Закись никеля поддается воздействию хлора медленнее, чем окись меди. С еще меньшими скоростями реагируют с хлором окись — закись кобальта и окись железа.
Устойчивость образующихся хлоридов в атмосфере кислорода (воздуха) также различна. При одинаковых температуре и составе газовой фазы сначала идет разложение кислородом хлорида кобальта, а затем хлоридов никеля и меди. Термодинамическая вероятность разложения хлорида железа очевидно еще выше, чем хлорида кобальта. Таким образом, окислы меди хлорируются полнее, чем окислы никеля, кобальта и железа. Хлориды меди при температурах обжига более устойчивы к воздействию кислорода, чем хлориды других металлов, входящих в состав файнштейна. Поэтому медь в огарке хлорирующего обжига в основном присутствует в форме легко растворимых хлоридов и оксихлоридов, а железо, кобальт и никель остаются преимущественно в виде нерастворимых окислов. Лишь незначительная часть кобальт и никеля в огарке содержится в форме устойчивых, хорошо растворяющихся сульфатов. Последние образуются в процессе обжига вследствие наличия в обжигаемом материале больших количеств закиси никеля, являющейся очень хорошим катализатором окисления сернистого ангидрида до серного, сульфатизирующего окислы металлов:
Me О + S03 ↔ Me S04. (62)
Существенное значение при разделении металлов в процессе последующего выщелачивания огарка слегка подкисленной водой имеет хорошая растворимость окислов меди в слабокислых растворах и практически полная нерастворимость в этих растворах «окислов железа, никеля и кобальта.
Восстановительная электроплавка закиси никеля
Процесс восстановления закиси никеля в электропечи описывается следующими реакциями:
NiO + CO=Ni + CО2
CО2 + C = 2СО
NiO + C = Ni + CO (63)
На основании экспериментального изучения равновесия реакции восстановления закиси никеля окисью углерода В. П. Богацкий вывел следующие уравнения для расчетов убыли энергии Гиббса и константы равновесия этого взаимодействия:
![]() = 51 000 – 96207Т-1 + 93Т lg Т - 256Т - 0,0203Т2+ 0,00000126Т3 Дж/моль; (64)
= 51 000 – 96207Т-1 + 93Т lg Т - 256Т - 0,0203Т2+ 0,00000126Т3 Дж/моль; (64)
![]() (65)
(65)
Ниже приведены значения константы равновесия, рассчитанные для различных температур:
Температура, °С: 500 600 700 800 900 1000 1100
Кр 554,6 310,8 192,7 130,9 96,93 73,87 57,2
Реакция восстановления закиси никеля окисью углерода в твердой шихте до ее расплавления относится к типу топохимических превращений, имеющих автокаталитический характер с четко выраженным максимумом скорости реакции на кривой скорость — время в кинетической области взаимодействия. Наличие максимума на кривых восстановления показано в работах Г. И. Чуфарова с сотрудниками. Однако, как известно, наличие максимума скорости еще не является доказательством автокаталитичности процесса и может свидетельствовать лишь о соответствующем изменении величины реакционной поверхности. Более убедительна автокаталитический характер реакции восстановления закиси никеля был показан В. В. Болдыревым и А. С. Ермолаевым. Они установили ускоряющее влияние свежевосстановленного никеля на ход процесса. Каталитическое действие никеля при этом объясняется тем, что он облегчает рост кристаллов новой фазы и вследствие заметного различия параметров решеток окисла и металла деформирует слой окислов и облегчает химический акт восстановления.
Помимо указанных реакций восстановления, при электроплавке может идти растворение закиси никеля в расплавленном металле, науглероживание металла и растворение образующегося карбида в металлической ванне. Вследствие этого имеет место-восстановление закиси никеля в жидкой ванне по реакции
Ni3C+NiO=4Ni+CO (66)
Реакция протекает очень интенсивно, сопровождается обильным выделением окиси углерода и часто приводит к хлопкам и выбросам расплава из печи. Растворимость углерода в жидком металлическом никеле достаточно высока. При науглероживании металла температура плавления никеля уменьшается, снижаясь до 1315°С для эвтектического сплава, содержащего 2,2% С. Поэтому в целях ускорения процесса плавления работают с избытком восстановителя, получая науглероженный металл. В процессе доводки избыток углерода легко удаляется присадкой в ванну закиси никеля.
Перед выпуском расплавленного никеля из электропечи для обессеривания металла в печь добавляют чистый известняк. При этом сера, присутствующая в ванне в форме сульфида никеля переходит в форму нерастворимого в металле сернистого кальция:
Ni3S2 + 2СаО + 2С = 3Ni + 2CaS + 2CO , (67)
который удаляется со шлаком. При наведении известковистого шлака печь работает частично по режиму сопротивления, отчего мощность дуги снижается. Слой шлака, покрывая ванну металла, предохраняет свод от воздействия высокой температуры, создаваемой открытой электрической дугой.
В процессе обезуглероживания ванны металл частично окисляется за счет вводимой закиси никеля. Поэтому при разливке металла в аноды с целью получения более плотных отливок иногда проводят раскисление ванны присадкой кремния. Образующийся при этом кремнезем переходит в шлак, который частично оставляют в печи и свертывают его магнезитовым порошком; после выпуска металла из печи шлак «садится» на лещадь, что приводит к ее наращиванию.
В состав шихты восстановительной электроплавки входят закись никеля, восстановитель, флюсы и оборотные материалы. В качестве восстановителя используют нефтяной кокс или другие углеродистые материалы с низким содержанием вредных примесей (S, Fe, As и т. д.).
Восстановительную электроплавку на отечественных предприятиях проводят в дуговых закрытых трехэлектродних наклоняющихся печах типа РНБ-2250, ДСТ-1300 и ОКБ-892.
Шихту в печь загружают через центральное отверстие в своде с помощью шнекового питателя, имеющего водоохлаждаемую конструкцию (для предотвращения спекания шихты). Газы из печи отводятся через кессонированный патрубок, установленный у края свода, и затем поступают под зонт, расположенный над патрубком.
Организация центральной загрузки позволила перейти на полунепрерывный процесс. Раньше каждая смена начинала плавку на пустой печи. При полунепрерывной плавке печь всегда заполнена металлом, на открытую поверхность которого непрерывно загружают шихту при максимальной токовой нагрузке. Загрузку шихты прекращают лишь в период доводки металла перед разливом никеля. После скачивания шлака заливают один круг изложниц, затем цикл плавки повторяют.
При работе с почти непрерывной загрузкой шихты на жидкую ванну прекратились выхлопы газов и выбросы шихты, сократились непроизводительные простои агрегата, возросли коэффициент использования печи под токовой нагрузкой (до 90% против 70— 75% при прежнем режиме работы) и производительность печи.
В последние годы большинство заводов перешло на плавку предварительно восстановленной закиси никеля, что также способствовало значительному увеличению производительности электропечей и снижению расхода электроэнергии на 1 т металла.
Перевод печи на шихту с предварительно восстановленной закисью никеля улучшил и другие показатели процесса. Уменьшилось газовыделение из печей, а следовательно, и безвозвратные потери металла. Сведены к минимуму выбросы расплава из печи. При повысившейся электропроводности шихты появилась возможность зажигания дуги непосредственно на шихте без обязательной загрузки скрапа, уменьшилось время для набора полной токовой нагрузки в период наплавления ванны. Два последних обстоятельства имеют особенно большое значение для печей, работающих в периодическом режиме.
Ниже приведены основные показатели восстановительной электроплавки закиси никеля:
Расход электроэнергии, кВт • ч/т никеля 1080—1180
Расход материалов, кг/т никеля:
графитированных электродов 15—20
восстановителя 125—170
известняка 5—28
огнеупорного кирпича 28—40
Извлечение никеля из закиси, % 99—99
Способы получения меди из рудного сырья
За рубежом в настоящее время пирометаллургическим способом производится около 85% от общего выпуска меди. В России на долю меди, производимой гидрометаллургической технологией, приходится менее 1%. Перспектив для значительного развития гидрометаллургии меди на ближайшие десятилетия в нашей стране нет.
Таким образом, переработку медного и никелевого рудного сырья в основном производят пирометаллургическими процессами.
К числу пирометаллургических процессов, применяемых при производстве меди относятся окислительный обжиг, различные виды плавок (на штейн, восстановительные, рафинировочные), конвертирование штейнов и в ряде случаев- возгоночные процессы.
Технологические схемы действующих предприятий по производству меди и никеля в каждом случае имеют свои специфические особенности, связанные с видом перерабатываемого сырья, применяемым металлургическим оборудованием, источниками тепловой энергии и с рядом других местных условий. Однако все они близки по своей структуре и укладываются в рамки принципиальных технологических схем.
С учетом разновидностей перерабатываемых медных и никелевых руд в настоящее время в промышленности используют три принципиальные пирометаллургические схемы.
Пирометаллургическую переработку сульфидных медных руд и концентратов можно вести двумя путями. Первый путь предусматривает полное окисление всей серы перерабатываемого сырья с помощью предварительнего окислительного обжига (обжиг «намертво») при одновременном переводе меди железа в оксидную форму:
4FeS2 + 11О2 = 2Fe2O3 + 8SO2;
2Cu2S + ЗО2 = 2Cu2O + 2SO2.
Продукт обжига (огарок) далее подвергают селективному восстановлению при полном расплавлении материала — восстановительной плавке. При этом медь восстанавливается до металлического состояния, а железо — в основном до вюстита. Оксиды железа совместно с пустой породой руды и оксидами флюсов образуют шлак, который удаляют в отвал. Процесс восстановления описывается следующими основными реакциями:
Си2О + СО = 2Си + СО2,
Fe2O3 + СО = 2FeO + СО2,
FeO+CO=Fe+CO2.
Такой прием получения меди кажется наиболее простым и естественным. Именно поэтому он, по существу, был единственным способом переработки медных руд в XVIII и XIX вв. Однако целый ряд существенных недостатков восстановительной плавки заставил отказаться от ее применения. В настоящее время процесс, близкий к восстановительной плавке, используется лишь для переработки вторичного медного сырья. Важнейшими недостатками этого метода являются:
1. При плавке получается очень грязная (черная) медь, содержащая до 20% железа и других примесей. Это, как известно из теории пирометаллургических процессов, объясняется облегченными условиями восстановления железа в присутствии расплавленной меди. Рафинирование черной меди от большого количества примесёй является очень сложным и дорогим и связано, кроме того, с большими потерями меди,
2. Шлаки, находящиеся в равновесии с металлической медью, получаются очень богатыми, что снижает извлечение меди в товарную продукцию.
3. Плавка осуществляется с большим расходом (до 20% от массы шихты) дефицитного и дорогого кокса.
Второй путь, характерный для современной пирометаллургии меди, предусматривает на промежуточной стадии технологии плавку на""Штейн" с последующей его переработкой на черновую медь. Пустая порода при этом переходит в шлак. Плавку на штейн можно вести в окислительной, нейтральной или восстановительной атмосфере. В условиях окислительной плавки можно получать штейны любого заданного состава. В этом случае преимущественно будут окисляться сульфиды железа с последующим ошлакованием его оксида кремнеземом по реакции
2FeS + ЗО2 + SiO2 = 2FeO • SiO2 + 2SO2. (14)
При плавке на штейн в нейтральной или восстановительной атмосфере регулировать степень десульфуризации невозможно и содержание меди в штейнах будет значительно отличатся от ее содержаниям в исходной шихте. По этой причине для получения более богатых по содержанию меди штейнов при переработке бедных концентратов иногда целесообразно предварительно удалить часть серы путем окислительного обжига, осуществляемого без расплавления материала при 800—900 °С.
Дальнейшую переработку штейнов с целью, получения из них металлургической меди осуществляют путем их окисления в жидком состоянии. При этом вследствие большего сродства железа к кислороду сначала окисляется сульфид железа по реакции (14). После окисления всего железа и удаления получившегося шлака окисляют сульфид меди по суммарной реакции:
Cu2S + О2 = 2Cu + SO2. (15)
Технология, включающая плавку на штейн, позволяет получать более чистый металл, содержащий 97,5—99,5% Си. Такую медь называют черновой. Рафинирование черновой меди по сравнению с черной значительно упрощается и удешевляется.
В последние годы в металлургии сульфидного сырья все большее развитие получают автогенные процессы, осуществляемые за счет тепла от окисления сульфидов при использовании подогретого дутья и дутья, обогащенного кислородом. В этих процессах, являющихся окислительными плавками, в одной операции совмещаются процессы обжига и плавки на штейн.
Современная пирометаллургия меди, несмотря на принципиальную общность используемых различными предприятиями технологических схем, предусматривает несколько вариантов (I—IV) ее практического осуществления (рис. 14).
Как следует из рис. 14, технология получения черновой меди характеризуется многостадийностью (за исключением варианта IV, предусматривающего непосредственную плавку концентратов на черновую медь). В каждой из последовательно проводимых технологических операций постепенно повышают концентрацию меди в основном металлсодержащем продукте за счет отделения пустой породы и сопутствующих элементов, главным образом железа и серы. На практике удаление железа и серы осуществляют за счет их окисления в три (обжиг, плавка, конвертирование), в две (плавка, конвертирование) или в одну стадию.
Наиболее распространенная до настоящего времени технология предусматривает (см. рис. 14) обязательное использование следующих металлургических процессов: плавка на штейн, конвертирование медного штейна, огневое и электролитическое рафинирование меди. В ряде случаев перед плавкой на штейн проводят предварительный окислительный обжиг сульфидного сырья.
Плавку на штейн медных руд и концентратов — основной технологический процесс — можно проводить практически любым видом рудных плавок. В современной металлургии меди для ее осуществления используют отражательные, руднотермические (электрические) и шахтные печи, а также автогенные процессы нескольких разновидностей.
Удельный вес различных способов производства меди в Советском Союзе выражается следующими примерными цифрами, %: 60—65 — отражательная плавка; 18—22 — шахтная плавка; 10—15 — электроплавка; 8—10 — автогенные процессы; 0,1—0,2 — гидрометаллургия.
Никель, полученный из окисленных руд, выпускают в гранулированном виде (огневой никель) без дополнительного рафинирования. Это обусловлено тем, что такой никель не содержит в больших количествах вредных для черной металлургии примесей и в основном его используют для легирования специальных сталей.
Технология переработки очень бедных окисленных никелевых руд, подвергающихся плавке на штейн без предварительного обогащения, очень громоздка и многостадийна, что является ее большим недостатком.
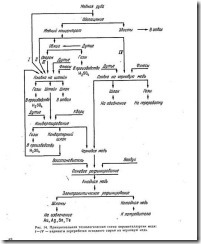
Основы электролиза криолитоглиноземиых расплавов
Производство алюминия основано на электрохимическом разложении глинозема, растворенного в криолитовом расплаве. Можно поставить два вопроса:
почему нельзя разлагать электролизом водные растворы солей алюминия, например нитраты, сульфаты и т.д;
почему не производить алюминий так же, как получается железо в печах при восстановлении оксидов, например по реакции
Fe2O3 + ЗС = 2Fe + ЗСО. (1)
Ответ на них дает второй закон термодинамики. Согласно этому закону вещества обладают особым внутренним энергетическим свойством (энергией Гиббса G), которое можно при электролизе изменить (увеличить), только совершив электрическую работу. Такая связь описывается уравнением
-ΔG = А*Q = Е°* z*F, (2)
где А — электрическая работа; Q — количество электричества; Е° — равновесная ЭДС; г — число электронов, участвующих в реакции; F — число Фарадея (96484 Кл/моль).
Величина Е° при разложении воды на водород и кислород при 25 °С составляет 1,229 В, тогда как реакция разложения
А12О3 = 2А1 + 1,5О2
требует ЭДС, равной 2,991 В. В этих условиях протекание тока приведет к осуществлению реакции с меньшим изменением энергии Гиббса (с меньшей ЭДС), т.е. к разложению воды.
Второй закон термодинамики утверждает, что система переходит самопроизвольно из первого состояния во второе, если во втором состоянии энергия Гиббса меньше, чем в первом. Между тем для реакции с использованием самого дешевого восстановителя — углерода
1-е состояние 2-е состояние
А12О3 + ЗС = 2А1 + ЗСО (3)
разница между энергиями Гиббса второго и первого состояний при достаточно высокой температуре 1000 °С (1273 К) составляет + 1090 кДж, и только при очень высоких температурах (более 2000 °С) разность становится отрицательной. Но при такой температуре резко увеличиваются эксплуатационные затраты, связанные с коррозией и износом оборудования. Вот почему промышленные способы термического получения алюминия до сих пор не разработаны, хотя попытки это сделать не прекращаются и поныне.
1.1. Электрохимический эквивалент — это число, показывающее, сколько граммов вещества выделяется на электроде (катоде или аноде) при протекании электродной реакции в расчете на единицу количества электричества (кулон или ампер • час). Рассмотрим способ его определения на примере реакций, протекающих на катоде и аноде алюминиевого электролизера.
В упрощенной форме основная катодная реакция присоединения электронов (восстановления) имеет вид
А13+ + 3е = А1. (4)
Уравнение (4) написано для отдельного атома. Умножим правую и левую части (4) на число Авогадро (число атомов и грамм-моле, N). Тогда количество веществ окажется выраженным в грамм-молях (М). Произведение е*N = F носит название числа Фарадея. Подставив величину заряда электрона (1,6*10-19 Кл) и числа Авогадро (N = 6,023 • 1023 моль-1), получим F = 96486 Кл ■ моль-1 (или 26,8 А • ч • моль-1). Тогда уравнение для расчета электрохимического эквивалента К будет иметь вид
К = М/3 • F. (5)
Подставив значение М = 26,97 г • моль 1 и F = 26,8 А • ч • • мель ~1 для восстановления трехвалентных ионов алюминия, получим К = 0,3354 г/ (А • ч).
В упрощенной форме анодная реакция примет вид
2О2- - 4е + С = СО2. (6)
Рассуждая аналогично, получим электрохимический эквивалент для углерода К - 12/4 • 26,8 = 0,112 г/(А • ч), для СО2 К = 36/4 • 26,8 = 0,336 г/(А • ч) и для кислорода К = 32/4 • 26,8 = 0,299 г/(А • ч).
1.2. Выход по току. Из размерности электрохимического эквивалента следует, что он определяет количество вещества Рт, получающегося при пропускании через электрод единицы количества электричества (ампер-часа или кулона). Чтобы рассчитать массу для случая произвольного количества электричества Q, надо электрохимический эквивалент К умножить на это количество электричества. Тогда получим;
Рт = К*Q = К* I*t, (7)
где I — сила тока; t — время.
Например, при / = 200 кА и t = 24 ч (т.е. сутки) имеем Рт = 0,3354*200•24 = 1612,8 кг/сут. На практике данная масса металла Рп отличается от теоретически рассчитанной.
Это отношение
η = Рп/Рт (8)
(где Рп — масса, определенная взвешиванием) называется выходом по току. При промышленном электролизе выход по току меньше единицы, и практически полученная масса с учетом (7) находится по уравнениюj
Рп = V К- I t. (9)
В промышленном электролизе выход по току зависит от множества факторов и составляет от 0,88 до 0,96.
1.3. Состав электролита. Расплавленный криолит (Na3AlF6), являющийся хорошим растворителем глинозема, — главный компонент электролита. Для снижения температуры начала кристаллизации и улучшения других свойств электролита (о чем подробнее будет изложено далее) в расплав. Водятся добавки, в частности соли или оксиды кальция, Магния и лития, а также фторид алюминия. Естественно, что в состав электролита входит и глинозем (от 1 до 8 % (по Массе)).
1.4. Устройство электролизера. Электролизер включает следующие основные блоки: 1 — катодное устройство, где протекает электролиз; 2 — анодный узел, где на подошв угольного анода происходит выделение анодных газов (реакция (6)); 3 — систему подвода тока (ошиновка); 4 — систему Ьиоотсоса. Схемы основных двух типов ванн: с самообжигающимся анодом (анодом Содерберга) и предварительно обож-Ьенным анодом (ОА) представлены на рис. 2.1 и 2.2 [3]. I Катодное устройство размещается в стальном кожухе длиной 9—14 м, шириной 3—4,5 м и высотой 1—1,2 м. Кожух футеруется теплоизоляционными и затем огнеупорными материалами. Внутренняя часть катодного устройства выкладывается угольными блоками. Заделанные в нижние (подовые) блоки стальные стержни служат для отвода тока.
Анодный узел включает собственно угольный анод (со стальной рубашкой для анода Содерберга) и систему сталеалюминиевых токоподводов. Постоянное напряжение поддерживается за счет перемещения анода домкратами, опускающими или поднимающими анодную раму, к которой зажимами крепятся анодные токоподводы.
В общую цепь (серию) последовательно включается 150— 200 электролизеров, которые соединяются ошиновкой. Напряжение на ванне в зависимости от типа и конструкции меняется от 3,9 до 4,5 В.
Анодные газы на электролизерах с верхним токоподводом (ВТ) собираются в газосборном колоколе, укрепленном по периметру анодной рубашки (см. рис. 1). В этом случае предусматривается частичное дожигание оксида углерода и смолистых веществ, выделяющихся при коксовании анода, в специальных горелках, смонтированных вместе с газосборным колоколом.
1.5. Электролиз. Электрический ток, проходя через электроды и электролит, выделяет на катоде алюминий (а в небольшом количестве в сплаве с ним натрий и кальций), а на аноде — диоксид углерода СО2. При этом полная электрическая работа А определяется выражением
А = U*I*t, (10)
где U — напряжение.

Рис. 2.7. Принципиальная схема электролизера с анодом Содерберга. 1 — газосборный колокол; 2 — анодные штыри; 3 — анодная масса; 4 -электролит; 5 — настыль; 6 — блюмсы; 7 — угольная подина; 8 — катодный кожух; 9 — огнеупоры и теплоизоляция.

Рис. 2.2. Схема электролизера с обожженными анодами.
1 — катодное устройство; 2 — анодные блоки; 3 — токоподводящая штанга; 4 — газосборное устройство; 5 — анодная ошиновка.
Отношение затраченной энергии (10) на количество проишеденного металла (8) называется удельным расходом шнергии W (кВт • ч/кг), который равен
W = U/k * η = U/0,3354η = 2,98 U/η. (11)
Величина W может составлять от 12,6 до 17,0 кВт • ч/кг А1 в зависимости от напряжения и выхода по току, которые обусловлены типом электролизера, силой и плотностью тока, составом электролита и другими параметрами.
На поверхности электролита образуется корка, которую приходится пробивать, чтобы загрузить глинозем. Существуют несколько способов загрузки. Наиболее современный способ предполагает расположение пробойников и бункеров с дозаторами вдоль продольных сторон для ванн с анодом Содерберга или по центру ванны с обожженными анодами. Одна система пробойник—дозатор устанавливается в расчете приблизительно на 40 кА тока. Частота загрузки 1—2 мин при до:»е, меняющейся от 200 г до 1 кг. Диаметр загрузочного отверстия в корке при этом составляет около 15 см.
На некоторых заводах используется загрузка, основанная М» разрушении корки вдоль всей продольной стороны ванны Или ее части. С помощью балки, закрепленной на ванне и приводимой в движение пневмоцилиндрами, корка со слоем глинозема толщиной около 10 см продавливается с шириной канала, равной примерно 20 см. При этом в ванну попадает приблизительно 40 кг глинозема в расчете на погонный метр канала. Такими же параметрами характеризуются и другие системы пробивки напольно-рельсовые машины с фрезой как рабочим органом, а также дизельные машинки, снабженные пневмопробойником. Недостатком систем с разрушением корки является попадание в расплав столь большого количества глинозема, что зачастую он не успевает полностью раствориться, уходя под металл и образуя осадок, осложняющий работу ванны.
Важная особенность электролизера — его дифференцированная теплоизоляция. Хорошо утепленная подина должна исключать кристаллизацию электролита и глинозема (появление "коржей"), которые становятся причиной многих технологических осложнений: повышение омического сопротивления из-за низкой проводимости твердого электролита, неравномерность тока в подине, появление горизонтальных токов в металле, вызывающих его интенсивную циркуляцию, и т.д. Поскольку подовые блоки имеют пористость около 20 % и эти поры заполнены электролитом, а солевой расплав хорошо смачивает углерод, получается, что металл снизу находится в некотором электролитном "чулке". Малая теплоизоляция вдоль бортов с угольными блоками (200 мм) или блоками из карбида кремния (50—70 мм) приводит к тому, что вдоль бортов как в электролите, так и в зоне металла существуют настыли, состоящие в основном из твердого криолита. Однако между настылью и металлом, высота (уровень) которого составляет от 15 до 45 см в зависимости от типа электролизера, существует слой жидкого электролита толщиной несколько менее 1 мм. Этот слой поддерживает связь между основным объемом электролита и электролитом, находящимся под металлом. Настыль играет важную роль в работе ванны:
- защищает блоки от разрушения; растворенный в электролите или жидкий металлический алюминий реагирует с углеродом с образованием карбида (А14С3), который растворяется в электролите. Настыль является единственной надежной защитой бортовых блоков;
- служит естественным регулятором температуры электролиза. При повышении температуры настыль растворяется, что приводит к уменьшению теплового сопротивления, увеличению тепловых потерь и падению температуры (рис. 3). Перегрев электролита и увеличение коэффициента теплообмена на границе электролит—настыль или металл—настыль снижают толщину настыли. Именно этим объясняется тот факт, что в этом районе всегда наблюдается самая тонкая настыль; растворение настыли или ее кристаллизация — одна из главных причин изменения состава электролита; 4) надлежащая настыль формирует форму рабочего пространства (ФРП), определяет небольшую скорость циркуляции Металла, при которой достигается высокий выход по току.
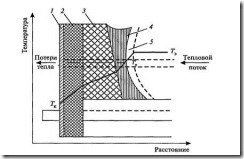
Рис. 2.3. Стационарный тепловой поток через бортовую стенку. / — кожух; 2 — теплоизоляция; 3 — бортовой блок; 4 — настыль; 5 — пограничный слой электролита; Тк — температура кожуха; Т„ — температура ликвидуса; Тэ — температура электролита.
Одним из жестких требований к современному электролизу является поддержание определенного расстояния анод—катод (МПР). Обычно МПР составляет 5—6 см, и каждый из них "стоит" приблизительно 350 мВ падения напряжения в электролите. Однако эти цифры не отражают особенностей технологии и всегда приходится доказывать необходимость даже очень небольшого уменьшения МПР (зажатия ванны) или, наоборот, ее разжатия. Грамотный специалист понимает, что Попытка необоснованно снизить МПР обязательно приведет к усилению волнообразования (потере устойчивости), а в конечном итоге — к снижению выхода по току. Увеличение МПР, повышая выход по току, одновременно вызывает рост напряжения и, следовательно, удельного расхода энергии.
В небольшом разделе, посвященном принципам электролиза, естественно, невозможно полностью осветить вопросы, связанные с эффективностью процесса. Если мерилом его эффективности принять расходные коэффициенты (энергии углерода, фторидов) в расчете на тонну алюминия, количество вредных выбросов и себестоимость передела, то окажется, что перечисленные величины зависят приблизительно от 100 характеристик исходных продуктов и 30 технологических параметров, зачастую тесно связанных друг с другом. Эту связь позволяют выявить статистические методы анализа, современные компьютерные методы нейронного анализа, аналитические зависимости и т.п. силлиманит (А12О3-SiO2), муллит (ЗА12О3 • 2SiO2) и др. В этом случае восстановлению подвергается также оксид кремния. При таком процессе получаются сплавы, содержащие, как правило, не более 60 % алюминия. Богатые по кремнию сплавы могут быть расшихтованы алюминием до силуминов, используемых в промышленности, которые содержат около 10 % кремния.
Алюминий может быть выделен из сплава растворением (экстракцией) такими металлами, как магний, ртуть, свинец, цинк при высоких температурах с последующей отгонкой металлов, имеющих высокую упругость пара.
Интересным методом выделения алюминия из сплавов является субгалогенидная дистилляция. Реакция взаимодействия алюминия с его фторидом
1200 °С 800 "С
2А1 (в сплаве) + A1F3 = 3A1F (пар) = 2А1 (жидкость) + A1F3 (15)
приводит при 1200 °С к образованию пара субфторида, который при 800 °С разлагается (диспропорционирует) на металл и трехвалентную соль. Сходные реакции, но при меньших температурах протекают при воздействии на алюминий его трихлорида.
Описанные (и многие другие) процессы термического восстановления и последующего рафинирования при всей их привлекательности пока не стали промышленными, не выдержав экономической конкуренции.
Сырье и основные материалы
В предыдущей главе показано, что при производстве алюминия электролитическим способом расходуются только глинозем и углерод анода. Среда (электролит), в которой идет процесс электролиза, состоит из криолита 3NaF * A1F3, фторидов алюминия A1F3, натрия NaF, кальция CaF2, магния MgF2 и др., суммарный расход которых не превышает 50—70 кг/т алюминия. Расход же глинозема на производство 1 т алюминия составляет около 2 т, и поэтому он является основным сырьем.
В чистом виде глинозема в природе нет, его получают из различных руд гидрохимическими способами. Представляет практический интерес кратко знакомиться с состоянием мировой базы для производства глинозема.
Основные минералы и руды алюминия
Алюминий широко представлен в земной коре различными соединениями, которые делятся по количеству видов примерно ил две равные группы:
первичные минералы, образующиеся при кристаллизации магмы. Главная роль в этой группе принадлежит алюмосиликатам — ортоклаз, альбит, лейцит и нефелин. Меньшее распространение имеют силикаты алюминия — дистен, силлиманит, андалузит, шпинели и свободный оксид алюминия — корунд; вторичные соединения алюминия, образующиеся под воздействием выветривания в земной коре, характеризуются 1)олее высоким содержанием оксида алюминия. Среди них широко распространены гидросиликаты алюминия, а также гидроксиды и оксигидроксиды алюминия — гиббсит, бемит и диаспор, которые являются важнейшей составной частью основных промышленных алюминиевых руд — бокситов. К этой же группе относится и алунит.
Боксит — сложная горная порода, состоящая из оксидов и гидроксидов Al, Fe, Si и Ti, а в качестве примесей присутствуют карбонаты кальция и магния, гидросиликаты (хлориты), сульфиды и сульфаты (в основном железа) и органические соединения. В природе мономинеральные бокситы чрезвычайно редки, гораздо чаще встречаются руды смешанного типа: гиббсит-бемитовые или бемит-диаспоровые.
Качество бокситов определяется содержанием в них А12О3 и SiO2, для чего используют кремниевый модуль μSi — массовое отношение содержания А12О3 к SiO2, т.е. чем выше модуль, тем лучше качество боксита. Разведанные запасы бокситов превышают 50 млрд т, что обеспечивает сырьем алюминиевую промышленность на многие годы. Основные месторождения остаточного типа расположены в тропическом и субтропическом поясах земли (табл. 3.1).
Основной особенностью этих месторождений является преобладание гиббситовых рудных тел с высоким кремниевым модулем, небольшая глубина залегания, позволяющая вести их добычу открытым способом, а также возможность обогащения отмывкой, что предопределяет высокую экономичность их переработки.
Залежи бокситов осадочного типа состоят из нескольких слоев, различающихся по модулю, а глиноземсодержащие соединения зачастую находятся в виде трудно перерабатываемого диаспора. Такие месторождения разрабатываются шахтным способом, и их обогащение затруднено. К сожалению, к этому типу относится большинство месторождений нашей страны.
Наиболее высококачественные отечественные бокситы домываются на Урале в Северо- и Южно-Уральских бокситовых рудниках (СУБР и ЮУБР) и перерабатываются в глиноземных цехах Уральского и Богословского алюминиевых заводов. Они добываются в сложных горно-геологических условиях на глубине до 1 км и относятся к трудновскрываемому диаспоровому типу. В этой связи себестоимость их добычи и переработки значительно выше, чем на многих зарубежных заводах.
Тургайские (Северный Казахстан) каолинит-гиббеитовые бокситы, имеющие низкий кремниевый модуль и высокое содержание сидерита FeCO3, являются основной сырьевой базой Павлодарского алюминиевого завода.
В Архангельской области ведется открытая разработка Северо-Онежских гиббсит-бемитовых бокситов с низким модулем и большим содержанием хрома, что исключает их переработку на глинозем по наиболее экономичному способу Байера.
Наиболее перспективными считаются Висловское (г. Белгород) и Средне-Тиманское (Республика Коми) месторождения бокситовых руд, которые могут быть относительно легко переработаны. В настоящее время активно ведутся работы по освоению месторождения бокситов в Республике Коми.
Нефелиновые руды, содержащие в качестве основной составляющей нефелин (Na,К)2О•А12О3•2SiO2, имеют большое значение для отечественной промышленности и перерабатываются на Пикалевском (ПОГ), Бокситогорском (БГЗ), Ачинском (АГК) глиноземных заводах.
При переработке нефелиновых руд и концентратов наряду с глиноземом получают поташ и соду, а из отходов глиноземного производства — цемент. Таким образом, нефелиновое сырье представляет собой комплексный продукт, но его переработка осуществляется по сложным технологическим схемам внедрение которых требует значительных капитальных вложений.
Добыча бокситов, производство глинозема и алюминия являются последовательными стадиями единого технологического процесса, но объем добычи бокситов, производство глинозема и алюминия по регионам не совпадают, о чем свидетельствуют данные за 1996 г.
Алюминиевая промышленность России, производящаяся около 3 млн т алюминия в год и занимающая второе место в мире после США, не располагает достаточными ресурсами высококачественных бокситов и мощностей по их переработке. В настоящее время пять глиноземных заводов России обеспечивают около 40 % потребности отечественных алюминиевых заводов, поэтому часть глинозема приходится завозить из-за рубежа.
Глинозем, используемый для производства алюминия, должен быстро растворяться в электролите, содержать минимально возможное количество оксидов железа, кремния и других более электроположительных, чем алюминий, элементов, так как, выделяясь на катоде вместе с алюминием, они ухудшают его качество. Нежелательно присутствие в глиноземе оксидов щелочных и щелочно-земельных металлов, поскольку они, вступают во взаимодействие с A1F3, разлагают и изменяют состав электролита, что вызывает необходимость его корректировки. Кроме того, оксид калия, проникая в угольную футеровку, снижает срок службы ванны.
При наличии оксида натрия Na2O в глиноземе происходит реакция
2A1F3 + 3Na2O = 6NaF + А12О3.
С увеличением содержания оксида натрия возрастает расход фторида алюминия.
При содержании соды в глиноземе более 0,33 % начинает и нарабатываться излишнее количество электролита, который приходится выливать из ванны, что влечет за собой увеличение себестоимости алюминия.
Крайне нежелательно присутствие влаги в глиноземе, так как при взаимодействии воды с криолитом и фторидом алюминия образуется фтористый водород HF:
2Na3AlF6 + ЗН2О = А12О3 + 6NaF + 6HF ↑;
2A1F3 + ЗН2О = А12О3 + 6HF ↑,
что приводит к дополнительному расходу фторидов. Как следует из этих реакций, из каждых 18 г воды, попавших в электролит, образуется 56 г HF.
У безводного оксида алюминия, каким является глинозем, известны и хорошо изучены две разновидности. Первая из них — а-А12О3, или корунд, — единственная форма безводного оксида алюминия, встречающаяся в естественных условиях. Все виды гидратов оксида алюминия при нагревании до 1200 °С превращаются в а-А12О3.
Вторая полиморфная разновидность безводного оксида алюминия, открытая в 1925 г., у-А12О3 (гамма-глинозем) в природе не встречается. При нагревании выше 900 °С он начинает превращаться в а-А12О3, и при температуре 1200 °С этот процесс завершается. Гамма-глинозем гигроскопичен, поэтому его содержание в техническом глиноземе лимитируется.
Физико-химические свойства глинозема зависят от исходного сырья и технологии его получения. Большое значение имеет удельная поверхность глинозема, которая увеличивается с уменьшением содержания а-А12О3. Снижение этого показателя приводит к ухудшению улавливания фтора при сухой очистке отходящих анодных газов.
За рубежом используют упрощенную классификацию глинозема по физическим свойствам, согласно которой он разделен на три группы: пылевидный (европейский, или мучнистый), песчаный (или американский) и недопрокаленный (или промежуточный), разработанный специально для использования в установках сухой очистки газов.
Большинство заводов США, Канады, Западной Европы используют песчаный глинозем, а отечественный ближе к недопрокаленному. Физические свойства глинозема влияют на такие показатели электролиза, как расход электроэнергии, глинозема, анода и фторидов, запыленность атмосферы в рабочей зоне, качество улавливания фтора при сухой газочистке и пр. Установлено, что скорость растворения у-глинозема существенно выше скорости растворения а-А12О3, однако при погружении у-А12О3 в электролит он практически мгновенно переходит в а-А12О3. Фазовый состав глинозема не оказывает заметного влияния на скорость его растворения, а повышение температуры электролита с 1010 до 1080 °С увенчивает скорость растворения примерно в 7 раз. Зарубежными исследователями установлено, что песчаный глинозем с содержанием 5 % а-А12О3 образует твердую, недопрокаленый — слабую корку, а мучнистый — не образует ее вовсе.
Как указывалось выше, основными составляющими электролитов являются криолит Na3AlF6 (3NaF-AlF3), A1F3 и А12О3. Кроме того, в электролит попадают вместе с сырьем или искусственно вносятся фториды кальция CaF2, магния MgF2, лития LiF и хлорид натрия NaCl. Основные свойства веществ, входящих в состав электролитов, представлены в табл. 3.8.
Наиболее распространенный способ получения криолита из плавикового шпата — кислотный. После разложения плавикового шпата CaF2 серной кислотой H2SO4 образуется фтористый водород HF и гипс CaSO4:
CaF2 + H2SO4 = 2HF + CaSO4.
Фтористый водород поглощается водой с образованием плавиковой кислоты. Для получения криолита в раствор плавиковой кислоты, очищенной от кремния, вводят необходимое количество гидрата окиси алюминия А1(ОН)3 и соды
Na2CO3:
6HF + А1(ОН)3 = H3A1F6 + ЗН2О,
2H3A1F6 + 3Na2CO3 = 2Na3AlF6 + 3CO2 + 3H2O.
Для получения фторида алюминия чистую плавиковую кислоту нейтрализуют гидратом окиси алюминия
3HF + А1(ОН)3 = A1F3 + ЗН2О.
При нейтрализации плавиковой кислоты содой или карбо-Ийшми лития, магния и бария получают используемые при tлсктролизе алюминия NaF, LiF, MgF2 и BaF2 соответственно.
Криолит 3NaF • A1F3 представляет собой комплексную соль из фторидов алюминия и натрия — гексафторалюминат натрия. В природе он встречается весьма редко, поэтому алюминиевая промышленность работает на искусственном криолите. Важный показатель этой соли — криолитовое отношение, т.е. молярное отношение NaF к A1F3. Теоретически модуль криолита равен 3 (3NaF/AlF3 = 3. Фторид алюминия очень летуч, так как отгоняется не плавясь. Для компенсации этих потерь и нейтрализации щелочи, содержащейся в сырье, криолит выпускают с пониженным модулем, т.е. с повышенным содержанием фторида алюминия.
Фторид алюминия A1F3 — летучий, гигроскопичный порошок белого или розоватого цвета, плотностью 2,88 г/см3.
Фторид натрия NaF представляет собой кристаллический или порошкообразный продукт белого или серого цвета, плотностью 2,79 г/см3, весьма гигроскопичен, поставляется в герметичной таре (стальные барабаны, полиэтиленовые мешки и т.д.), на заводе хранится в закрытых складах. Ядовит, поэтому на упаковку наносят надпись "Яд".
1.4. Анодные материалы
В современных электролизерах используются два вида анодных материалов: самообжигающиеся аноды формуются из анодной массы, а для электролизеров с обожженными анодами используются предварительно прокаленные анодные блоки. Технология производства анодной массы и анодных блоков изложена ниже.
3.4.1. Анодная масса выпускается в России в соответствии с ТУ 48-5-80-86. Анодную массу изготавливают из пекового или нефтяного коксов. Масса, изготовленная из пекового кокса, лучше по прочности, пористости, удельному электросопротивлению, чем масса на основе нефтяного кокса, но пековый кокс дефицитен и дороже.
Анодные массы, предназначенные для электролизеров с БТ и ВТ, различаются только коэффициентом текучести. Масса для анодов с ВТ должна быть более текучей, чтобы она могла хорошо затекать в надштыревые отверстия при перестановке штырей, поэтому в ней содержится больше связующего, чем в массе для анодов с БТ. Все остальные требования к качеству анодной массы одинаковы для обоих типов электролизеров. Для электролизеров БТ выпускают "сухую" анодную массу, коэффициент текучести которой находится в пределах 1,2—1,8. Эти массы обозначены как АМС-0 и АМС-1.
На КрАЗе в последние годы успешно внедрена технология "полусухого" анода, для которой используются несколько видов масс, различающихся в основном текучестью.
Содержание золы в массе влияет на содержание примесей в алюминии, так как на производство 1 т алюминия расходуется более 500 кг анодной массы. В свою очередь, зольность массы определяется качеством коксов, а также износом технологического оборудования и, прежде всего, футеровки прокалочньгх печей.
Содержание серы в массе зависит от ее содержания в коксах. В нефтяных коксах содержание серы достигает 4 %, однако для производства анодной массы не рекомендуется использование кокса с содержанием серы более 1,5 %, в основном из экологических соображений.
Удельное электросопротивление (УЭС) массы и ее пористость — взаимозависимые величины: с увеличением пористости возрастает УЭС и увеличиваются потери электроэнергии в аноде.
С уменьшением пористости повышается механическая прочность анода, но она больше зависит от гранулометрического состава сухой шихты, содержания и качества связующего. Повышение механической прочности анода полезно лишь до определенного предела, так как с ее увеличением растет хрупкость анода, что влечет за собой образование трещин и сколов.
Общая разрушаемость в атмосфере углекислого газа характеризует поведение анода при воздействии на него СО2, выделяющегося в процессе электролиза. Разрушаемость анода состоит из суммы двух составляющих: окисляемости и осыпаемости. Окисляемость численно равна тому количеству углерода, которое расходуется при окислении анода углекислым газом (реакция Будуара: С + СО2 = 2СО). Чем меньше эта составляющая, тем меньше расход анода в процессе электролиза. Осыпаемость частиц кокса-наполнителя происходит в результате более высокой реакционной способности кокса из связующего. Данный показатель характеризует качество кокса из связующего, и чем он меньше, тем меньше расход анода.
Содержание влаги в массе не является браковочным показателем, а определяется для взаиморасчетов потребителей с поставщиками. Повышенная влажность может повлечь I вспучивание анодной массы в процессе ее расплавления в аноде.
Пористость массы зависит от ряда факторов: вида и качества исходного кокса, его гранулометрического состава, содержания и качества связующего, технологии обжига анода и пр. Большое влияние на качество анодной массы оказывает фанулометрический состав коксовой шихты, особенности которого рассмотрены далее.
2.2. Анодные блоки на современньгх электролизерах используют шириной 400—900, высотой 470—650 и длиной I 550—1600 мм. На заводах СНГ, оборудованных мощными I электролизерами (СаАЗ, ТадАЗ, КрАЗ), применяют анодные блоки шириной 700, длиной 1450 и высотой 600 мм. Изготавливают два сорта анодных блоков — АБ-0 и АБ-1. Для электролизеров Волховского алюминиевого завода используют анодные блоки меньших размеров, изготавливаемые Днепровским (ДЭЗ) и Новочеркасским (НЭЗ) электродными заводами.
На поверхности блоков допускается не более двух трещин шириной до 1 и длиной до 250 мм и сколов в нарезке ниппельного гнезда. Не допускаются трещины в ниппельном гнезде шириной более 0,5 и длиной 50 мм, а также вырывы, выпеки и сколы глубиной более 25 мм.
Углеродные футеровочные материалы
3.5.1. Подовые блоки. Шахту электролизера выполняют из углеродных блоков, так как они являются практически единственным материалом, способным противостоять воздействию расплавленного алюминия и электролита и хорошо проводить электрический ток.
Используемые в промышленности катодные блоки изготавливают из различных углеродных материалов и классифицируют следующим образом.
Графитированные блоки изготавливают из графитизируемых материалов, подвергают термообработке обычно до 3000 °С, в результате чего образуется графитообразный материал.
Графитизированные блоки изготавливают из графитизируемых материалов и прокаливают до 2300 °С.
Полуграфитовые блоки состоят из графитизированного наполнителя, но коксовое связующее обожжено до 1200 °С.
4. Антрацитовые блоки изготавливают из антрацита, иногда с небольшими добавками графита и обжигают при температуре 1200 °С. Этот вид блоков можно подразделить на три группы:
- антрацит равномерно обожжен газом или в печи и его графитация не происходит;
- антрацит обжигается электрическим током и в некоторой степени графитизируется;
- антрацит с добавками (до 30—50 %) графита.
Графитированные блоки очень дороги и поэтому применяются крайне редко, а полуграфитовые блоки, имеющие практически такие же показатели, как графитированные, не так дороги и используются достаточно широко.
С точки зрения срока службы подин стойкость к термическому удару — весьма важный показатель при обжиге ванн после капремонта. Теплопроводность подового блока не имеет большого значения, так как основные потери тепла от ванны идут через ее бортовые стенки.
В принципе нет разницы в конструкции катода для электролизеров с самообжигающимися и обожженными анодами.
Однако на ваннах с самообжигающимися анодами в подавляющем большинстве случаев загрузка глинозема в электролит происходит путем разрушения корки, при этом теряется большое количество тепла. На таких ваннах можно использовать в качестве бортовой футеровки блоки из антрацита (с низкой теплопроводностью), а на ваннах с предварительно обожженными анодами, которые, как правило, оборудованы системами автоматического питания глиноземом (АПГ), необходимы бортовые блоки с более высокой теплопроводностью во избежание перегрева расплава.
Блоки из углерода в процессе эксплуатации графитируются и примерно через год приобретают свойства, незначительно отличающиеся по тепло- и электропроводности от графитированной футеровки.
В России в соответствии с ТУ 1913-109-021-99 подовые блоки выпускают марок ПБ и ПБП ("подовый блок" и "подовый блок пропитанный" соответственно). Длина блоков 800— 3400 мм. Цифра после обозначения марки означает удельное электросопротивление в микроомах на метр.
3.5.2. Бортовые блоки. На современных отечественных электролизерах бортовую футеровку собирают из предварительно обожженных плит, изготовленных из тех же материалов и по той же технологии, что и подовые блоки. Однако свойства бортовых блоков, как показано выше, должны отличаться от свойств подовых блоков, так как они не предназначены для прохождения через них тока. Бортовые блоки должны обладать низкой электропроводностью и высокой теплопроводностью (с целью создания надежных бортовых настылей), т.е. нчаимоисключающими характеристиками. Бортовые блоки также должны быть стойки к воздействию расплава и не окисляться воздухом, не растворяться в криолите и алюминии и не смачиваться этими компонентами, иметь низкую пористость, стоимость, быть просты в изготовлении и технологичны при монтаже. Бортовая футеровка электролизеров с обожженными анодами и системой автоматического питания глиноземом может быть более тонкой, поскольку она менее подвержена механическому воздействию инструмента при пробивке корки электролита. Для бортовой футеровки, несмотря на ее невысокую стойкость к окислению воздухом и расплавом, до сих пор предпочтение отдается углеродным блокам из-за их дешевизны.
Из практики известно, что бортовая футеровка вследствие окисления воздухом и отходящими анодными газами, а также воздействия электролита и механических повреждений при обработке корки служит значительно меньше, чем подовые блоки. Поэтому ведется поиск огнеупорных материалов, пригодных для футеровки электролизеров и обеспечивающих длительный срок службы.
Бортовые блоки на основе карбида кремния SiC показали хорошие эксплуатационные свойства, однако их широкое применение сдерживалось более высокой стоимостью, чем углеродных. Кроме того, монтаж плит на основе карбида кремния проводили с помощью пекового связующего, что не позволяло полностью использовать преимущества этого материала. По некоторым данным, высокую коррозионную стойкость бортовой футеровки можно достичь только путем применения карбидо-кремниевых плит в сочетании с керамическим связующим. В настоящее время такая футеровка используется и на некоторых отечественных заводах.
В России выпускаются бортовые блоки марок ББ и ББП ("блоки бортовые" и "блоки бортовые пропитанные"). Толщина всех блоков 200, ширина 550, длина 400—800 мм, что позволяет монтировать шахту разной глубины. По этим же ТУ изготавливают и угловые блоки.
3.5.3. Подовая масса служит для набойки межблочных и периферийных швов, а также для накатки подушки на цоколь под подовые блоки. Ее изготавливают по разной рецептуре из антрацита, графита или прокаленного кокса, а в качестве связующего используют каменноугольную смолу, пек, полимеры. По температуре ее пригодности к набойке Х.А. Ойя различает горячую (140—180 °С), теплую (30—50 °С) и холодную (около 20 °С) массы. При использовании горячей массы условия набойки швов весьма тяжелые, что негативно сказывается на их качестве. При использовании теплой и холодной массы большинство негативных моментов, присущих горячей массе, исключаются, благодаря чему холоднонабивная подовая масса получила широкое распространение. При производстве теплой и холодной массы в связующее вещество добавляют летучие модификаторы, вследствие чего срок хранения массы ограничен.
Важнейшими свойствами подовой массы, влияющими на срок службы катода, являются уплотняемость в процессе набойки, степень усадки или расширения после обжига, качество наполнителя и связующего.
Огнеупорные и теплоизоляционные материалы
Теплоизоляционные и огнеупорные материалы используют в катодном устройстве электролизеров для снижения потерь тепла, предохранения катодного кожуха от воздействия высокой температуры и, в конечном итоге, для повышения срока службы электролизеров. По назначению эти материалы делят на:
материалы для подложек под катодные блоки (барьерные материалы);
огнеупорные материалы, устанавливаемые под катодными блоками и воспринимающие на себя воздействие проникающих фторидов;
теплоизоляционные материалы, снижающие потери тепла.
Очевидно, что все перечисленные требования не могут быть представлены в одном материале. Поэтому для каждого материала разработаны соответствующие требования.
3.6.1. Барьерные материалы служат мягкой подложкой под катодные блоки и препятствуют проникновению компонентов расплава в нижние слои футеровки. В качестве таких материалов применяют подушки из подовой массы, глинозема и 1 других материалов. Однако до настоящего времени нет единого мнения о наиболее предпочтительных барьерах, поэтому на отводах используют различные материалы для подложек. В последние годы за рубежом в качестве барьеров используют два типа порошков:
— тип А, основанный на анортите, СаО • А12О3 • 2SiO2;
— тип Б, основанный на оливине MgO • SiO2.
3.6.2. Огнеупорные материалы должны обеспечивать медленное проникновение криолитоглиноземных расплавов, сохранять форму и объем, а также исключать попадание электролита в зону расположения теплоизоляции.
Данным требованиям удовлетворяет множество материалов. Так, на КрАЗе в широком масштабе испытывались электролизеры с глиноземной изоляцией, но, несмотря на ряд преимуществ, они не нашли широкого применения.
В настоящее время для этих целей широко используют шамот — алюмосиликатный материал, содержащий 28—45 % А12О3, который дешевле других огнеупоров. В России широкое распространение получил кирпич различных размеров марки ШБ (ГОСТ 390-96), который содержит не менее 28 % А12О3, имеет огнеупорность не ниже 1650 °С и открытую пористость не более 30 %. В зарубежной практике находят применение муллитовые изделия с содержанием глинозема более 45 %. Теплоизоляционные материалы предназначены для снижения тепловых потерь и, следовательно, они должны обладать низкой теплопроводностью. Для этой цели используют различные материалы: диатомит, вермикулит (вспученная слюда с различной плотностью), силикат кальция (СаО • SiO2) и силикат алюминия—кальция (СаО • А12О3 • SiO2). В России широкое распространение для этих целей получили диатомитовые изделия, в том числе диатомитовый кирпич марок Д-500 и Д-600. В зарубежной практике, а в последние годы и на отечественных заводах применяют вермикулит различных типов, отличающийся в основном объемной плотностью.
Ток подводят к ванне металлическими проводниками — алюминий, медь, сталь, а анод и подина ванны выполнены из углерода, который также является проводником тока.
В современных электролизерах медь почти не применяют из-за ее дефицитности и высокой стоимости. Указанная максимальная температура является предельно допустимой, при которой сохраняются механические свойства и электропроводность. Электрическое сопротивление стали примерно в 5 раз выше, чем у алюминия, и ее используют для подвода к аноду и отвода тока от подин, поскольку нет более подходящего материала, который работает при температуре до 1100 оС.
Отношение теплопроводности к электропроводности у всех металлов практически одинаково, а у углерода оно в 35—40 раз больше. Это значит, что применять углерод для длинных токоподводов нерационально, т.е. ток к расплаву следует подводить короткими углеродистыми проводниками.
Корректировка состава электролита
В России принято оценивать состав электролита молярным соотношением основных компонентов криолита NaF/AlF3, которое называют криолитовым отношением (КО). За рубежом часто используют массовые отношения этих компонентов.
Криолитовое отношение определяет такие важные параметры электролита, как температуру его кристаллизации, растворимость в нем глинозема, электропроводность и другие параметры. Следовательно, поддержание КО на заданном уровне — одна из основных задач технологического персонала.
В течение многих лет считалось, что наиболее экономически выгодным значением КО является 2,6—2,8. Однако в последние годы большинство зарубежных заводов работают на "кислых" электролитах с КО = 2,4—2,6, что позволило им резко поднять технико-экономические показатели электролиза и снизить расход электроэнергии. Этот положительный опыт, теоретические основы которого изложены в гл. 4, активно внедряется и на отечественных заводах.
Рассмотрим причины изменения криолитового отношения. Как известно, основу электролита составляет криолит Na3AlF6, представляющий двойную соль NaF и A1F3. Молярное отношение фторида натрия к трифториду алюминия равно 3, а у промышленного электролита поддерживается в пределах 2,4—2,8. Состав электролита (КО) непостоянен во времени, так как при пуске ванны футеровка интенсивно пропитывается фторидом натрия, при этом значение КО падает, а электролит закисляется. В такой период для доведения КО до заданных значений в электролит добавляют фторид натрия. В процессе эксплуатации идет интенсивная возгонка трифторида алюминия с образованием HF, что приводит к повышению КО. Для компенсации потерь трифторида алюминия в заводской практике используют криолит с модулем не более 1,8.
Для расчета количества трифторида алюминия Сфа (кг), необходимого для корректировки состава электролита, пользуются формулой И.П. Гупало:
Сфа = 2m(К1 - К2)/с(2 + K1)K2,
где K1 и К2 — КО электролита соответственно до и после корректировки; т — масса корректируемого электролита, кг; с — содержание A1F3 в промышленном трифториде алюминия, доли ед. Масса электролита т обычно известна для каждого типа ванн.
Трифторид алюминия насыпают на корку электролита, прикрывают глиноземом, который адсорбирует фтор, выделяющийся при возгонке A1F3, и погружают в электролит при очередной обработке ванны.
Для быстрого наплавления электролита применяют флотационный и регенерационный криолит, который по своему составу близок к электролиту, поэтому его широко используют и на пуске ванн, и в процессе нормальной эксплуатации. Фторид натрия, как и трифторид алюминия, насыпают на корку и прикрывают глиноземом, но при слабых настылях фторид натрия лучше загружать у борта ванны. Обычно фторид натрия используют при пуске ванны, а при нормальной эксплуатации его специально не вводят, так как натрий содержится в виде примесей в сырье.
Как уже отмечалось выше, на ряде заводов используют фторглиноземную шихту, применение которой упрощает корректировку электролита.
При работе на низком криолитовом отношении для корректировки электролита применяют не криолит, а трифторид алюминия, который, взаимодействуя с оксидом натрия Na2O, неизбежно присутствующим в глиноземе, образует фторид натрия.
В настоящее время единственным способом извлечения жидкого алюминия из ванны является вакуумная выливка. Применяемый для этой цели вакуум-ковш (рис. 7.7) представляет собой герметичный сосуд в форме усеченного конуса, футерованный изнутри огнеупорным материалом. На грузовой траверсе ковша крепится механизм его поворота. Заборная труба соединена с ковшом шаровой опорой, которая предотвращает до некоторой степени поломку носков при ударах. Разрежение в ковше создается вакуум-линией, с которой ковш соединяют шлангами. На некоторых заводах на вакуум-ковшах устанавливают инжекторно-вихревые насосы, работающие от сети сжатого воздуха. На зарубежных заводах используют вакуум-ковши, транспортируемые тракторами или погрузчиками, что облегчает работу мостовых кранов.
Выливку металла из электролизеров БТ и ВТ производят, как правило, один раз в двое суток, а на мощных электролизерах ОА (255 кА) — ежедневно. Емкость вакуум-ковшей составляет 3 и 5 т, что позволяет проводить выливку металла из двух ванн в один ковш. Технологически это неудобно, но дает заметное снижение нагрузки на мостовые краны, которые всегда загружены.
Перед выливкой проверяют состояние ванны, замеряют уровни металла и электролита, величину осадка. За 5—10 мин до выливки в установленном месте для ввода вакуум-носка пробивают корку электролита, но не топят ее, а извлекают наверх, снимают пену, очищают подину от осадка и подгребают его к борту.
Выливщик вводит вакуум-носок в летку, подключает ковш к вакуум-линии и через смотровое стекло следит за запол нением ковша металлом. Электролизник в это время опускает анод, сообразуясь со скоростью выливки и не допуская превышения напряжения на ванне более чем на 0,1—0,2 В выше нормального. На некоторых заводах эту функцию выполняет система АСУТП. После выливки заданного количества металла отсоединяют шланг от ковша, извлекают носок из летки и вакуум-ковш транспортируют на средний проход, где жидкий металл переливают в разливочный ковш.
Такая технология выливки и транспортировки металла в литейное отделение несовершенна и имеет следующие основные недостатки:
- при переливке жидкого металла из вакуум-ковша в разливочный угар металла достигает 1 кг/т алюминия;
- конструкция вакуум-ковша не позволяет механизировать операции по его чистке;
- высота транспортных ковшей зачастую превышает высоту приемных карманов миксеров, что увеличивает длину открытой струи металла и повышает его угар;
- наличие вакуумных и разливочных ковшей увеличивает парк оборудования и затраты на его эксплуатацию и пр.

Рис. 7.7. Вакуум-ковш.
1 — сливной носок; 2 — люк; 3 — траверса; 4 — поворотный механизм; 5 — крышка; 6 — заборная труба; 7 — футеровка.
Для устранения указанных недостатков сотрудниками ИркАЗ совместно с СибВАМИ разработан вакуум-ковш со съемной крышкой (рис. 7.8), который совмещает функции вакуумного и транспортного ковшей. Длительные испытания показали высокую работоспособность таких ковшей, поэтому они нашли применение на некоторых заводах России.

Рис. 7.8. Вакуум-ковш со съемной крышкой.
1 — корпус; 2 — зажим; 3 — траверса; 4 — крышка; 5 — откидной носок; б — поворотный механизм; 7 — вакуум-носок.
На производство 1 т алюминия расходуется более 2,5 т различного сырья и материалов, поэтому транспортно-технологическая схема (ТТС) завода обусловлена масштабами производства и номенклатурой выпускаемой продукции. ТТС охватывает основные (электролизные, глиноземные и электродные), ремонтные и вспомогательные цехи, но из этого большого и сложного хозяйства рассмотрим только часть, касающуюся электролитического производства алюминия.
Транспортно-технологическая схема цеха электролиза
Технический уровень транспортно-технологических схем электролизных цехов определяется типом, производительностью и конструкцией основного технологического оборудования электролизеров.
В настоящее время погрузоразгрузочные операции (ПРО) и внутризаводские перевозки сырья и материалов в основном механизированы и частично автоматизированы, но для выполнения ряда операций используется еще немало ручного труда. Упрощенная ТТС электролитического производства алюминия v применением электролизеров с СОА приведена на рис. 10.1.
Рассмотрим методы приема, разгрузки и доставки в корпуса электролиза глинозема — наиболее массового вида сырья.
Приемные склады глинозема и фторидов. Глинозем и фториды поставляются железнодорожным транспортом в вагонах типа "хоппер" или в специальных цистернах. Наиболее распространенная схема приема и разгрузки этих видов сырья показана на рис. 10.2. Глинозем, поступающий в вагонах типа «хоппер", разгружается самотеком в приемный бункер, расположенный под железнодорожными путями склада, а оттуда пневматическим аппаратом 1 с помощью сжатого воздуха низкого давления перекачивается в складской силос 2. Эти аппараты (пневмоподьемники) способны перемещать глинозем вертикально или под некоторым углом вверх. Разгрузка глино-1сма из специализированных цистерн осуществляется в тот же силос пневматической системой, смонтированной внутри цистерны. Под складским силосом установлены пневматические насосы 1, перекачивающие глинозем в межкорпусные силосы 3. Пневматические насосы, установленные под бункерами приемного склада глинозема и под складскими силосами, имеют только наружное сходство, а их внутреннее устройство различно.
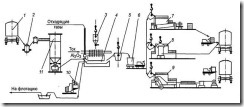
Рис. 10.1. Транспортно-технологическая схема производства алюминия.
1 — вагон (цистерна); 2 — пневмоподьемник; 3 — подача анодной массы; 4 — электролизер; 5 — вакуум-ковш; 6 — литейный ковш; 7 — разливка алюминия в чушки; 8 — литье слитков; 9 — производство катанки; 10 — угольная пена; 11 — межкорпусный силос глинозема.
Комплекс насосов, трубопроводов и межкорпусных силосов образует систему внешнего пневмотранспорта глинозема. Из межкорпусных силосов глинозем развозится специальными машинами по электролизерам, а на современных заводах для этой цели используют автоматизированную систему раздачи глинозема (ЦРГ), которая транспортирует его в бункеры, установленные на ваннах.
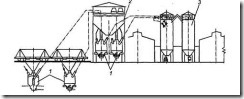
Рис. 10.2. Схема транспортировки глинозема. 1 — пневмоаппарат; 2 — складской силос; 3 — межкорпусные силосы.
Аналогично производится разгрузка и транспортировка фторидов (криолита и трифторида алюминия), но их грузопоток составляет лишь 3—5 % от объема поступающего глинозема. На некоторых заводах фториды поставляются в мешках или мягких контейнерах массой от 20 до 1000 кг, которые доставляют в корпуса электролиза авто- или электротранспортом. Склады глинозема полностью механизированы, а многие автоматизированы, поэтому затраты труда на них невелики и сводятся в основном к уборке просыпавшегося материала.
Транспорт анодной массы. Анодную массу на крупных заводах (БрАЗ, КрАЗ, НкАЗ, ИркАЗ, ВгАЗ, БАЗ) изготавливают в цехах анодной массы (ЦАМ), а на небольшие заводы (УАЗ, НАЗ, КАЗ) ее доставляют железнодорожным транспортом и разгружают самотеком из полувагонов в крытые склады. Крупногабаритные брикеты массой около 1,0—1,5 т разгружают мостовым краном. Подавляющее большинство заводов изготавливает анодную массу в виде мелких брикетов различной формы, массой около 0,2 кг. Лишь на БАЗе производят крупногабаритные брикеты, которые отправляют и на другие заводы. Разгрузка анодной массы механизирована, но возникают трудности, связанные со смерзанием массы зимой и с ее слипанием в жаркое время года.
Склады ремонтных материалов. Сырье и материалы для ремонта основного технологического оборудования (электролизеры, миксеры, прокалочные печи и пр.) представляют собой штучные грузы, состоящие в основном из угольных и огнеупорных материалов, хранение которых на открытом воздухе недопустимо. Состояние складского хозяйства, особенно на старых заводах, и погрузоразгрузочная техника не везде отвечают современным требованиям, что негативно влияет на качество ремонтов.
Для механизации погрузоразгрузочных операций и сохранности материалов большое значение имеет контейнеризация грузов и пакетирование, особенно для огнеупорных материалов. Незначительное увеличение стоимости пакетированного груза быстро окупается и снижает трудозатраты.
Для механизации ПРО используют авто- и электропогрузчики, мостовые и автомобильные краны, электрокары. Шамотный порошок, гипс, цемент разгружают самоходными разгрузчиками в специальные отсеки, оборудованные в складах, но нередко эти операции выполняют вручную. Подачу материалов на ремонтные объекты (ЦКР, литейное отделение или в корпуса на капитально ремонтируемые ванны) осуществляют автотранспортом и мостовыми кранами.
Склады вспомогательного производства предназначены для хранения каустической и кальцинированной соды, гидрата окиси алюминия. Кальцинированная сода поступает в крытых нагонах навалом или в бумажных мешках, а ее разгрузку ведут с помощью передвижных транспортеров или авто- и электропогрузчиков. Каустическая сода поставляется в жидком виде и сливается в специальные баки. Гидрат окиси алюминия доставляют в полувагонах в виде пасты и его разгрузка, особенно в зимнее время, представляет определенные трудности.
Хранение и доставка материалов и сырья для ремонтных и вспомогательных цехов в недостаточной степени механизирована, что приводит к значительным потерям дорогостоящих материалов.
Способы очистки отходящих газов
В отходящих газах содержатся пары, капли жидкости и частицы твердой пыли. При охлаждении пары конденсируются в аэрозоли и сгущаются в субмикронные агрегаты частиц сложного состава. По данным, в газах обнаружены следующие частицы и газы:
частицы: С, А12О3, Na3AlF6, Na5AlF14, A1F3, CaF2, углеводороды;
газы: HF, CF4, C2F6, SiF4, SO2, H2S, CS2, COS, CO2, CO, H2O, углеводороды.
Содержание этих примесей в отходящих газах зависит от типа электролизеров, технологических операций — обработка электролизеров, выпивка металла, замена анодов, регулирование положения анода и пр.
В твердых частицах больше всего содержится А12О3 и
фторидов. В газах преобладают СО и СО2, а также фториды; объем SO2 зависит в основном от количества серы в аноде. Наибольшую опасность представляют фториды и главным образом HF, количество которого в газах доминирующее.
Анализируя состав примесей, можно сделать вывод, что отходящие газы необходимо очищать от пыли, фторидов и при необходимости от SO2.
Очистка газа от пыли осуществляется следующими способами сепарации частиц из газового потока.
Устройства, работа которых основана на использовании силытяжести, — пылевые камеры, азоходы малоэффективны в электролизных цехах, так как для снижения скорости газа необходимо резко увеличивать диаметр газоходов, а при больших скоростях в пылевых камерах и газоходах будут оседать только крупные частицы, т.е. степень очистки газа будет невысокой.
Аппараты, основанные на использовании центробежной силы, — циклоны не могут эффективно применяться в цехе электролиза из-за больших объемов газа. Кроме того, они эффективны лишь для отделения крупных частиц.
Мокрые пылеуловители — скрубберы и пенные аппараты. Принцип работы этих аппаратов основан на смачивании частицы жидкостью, в результате чего они улавливаются. Опыт показывает, что при мокром улавливании газы хорошо очищаются от крупных частиц (>3—5 мкм), а мелкие частицы и возгоны улавливаются хуже, даже в том случае, если они по своей природе хорошо смачиваются жидкостью.
Скоростные мокрые пылеуловители дробят жидкость на мелкие капли, благодаря чему частицы легче сталкиваются с ними и лучше улавливаются. Они обладают рядом преимуществ: возможность очистки горячих газов, небольшие габариты, пониженная пожаро- и взрывоопасность. В то же время эксплуатация этих аппаратов, которые широко используются в электролизных цехах, особенно в зимнее время года, представляет большие сложности, так как необходимо обрабатывать и удалять большое количество стоков и шлама.
Очистка газа от фтористых соединений. Система очистки газов от фтористых соединений должна обладать высокой надежностью и работать с большой эффективностью. По западным нормам [10] ее КПД по улавливанию фтора должен составлять не менее 98,5 %. Для достижения такого уроним эффективности системы должны быть приспособлены дни улавливания газообразных и мелкозернистых частиц фторидов. Для этого часто применяют мокрый скруббер или двухступенчатую очистку в электрофильтре и мокром скруббере.
Соединения кальция и натрия добавляют в раствор дин улучшения улавливания газообразных фторидов. При использовании извести происходит реакция
СаО + 2HF = CaF2 + Н2О,
т.е. образуется водонерастворимый дифторид кальция CaF2, который без опасений может быть удален в отвал. На некою рых норвежских заводах, используя этот метод, полученный шлам сливают в океан, не опасаясь его загрязнения. Однако применение извести часто приводит к бразованию отложений из нерастворимых продуктов, в результате чего понижаем и надежность и требуются большие эксплуатационные затршы И России применяют растворы натриевых соединений. При использовании раствора кальцинированной соды Na2CO3 протекает реакция
HF + Na2CO3 = NaF + NaHCO3.
Наличие в отходящих газах оксида серы SO2 приводит к образованию сульфата натрия
SO2 + О2 + Na2CO3 → Na2SO4 + СО2,
в связи с чем полученный из растворов газоочистки криолита всегда будет загрязнен сульфатом натрия.
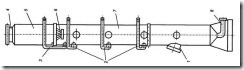
В России на большинстве заводов используется мокрый способ очистки газов от фтористых соединений, в то время как в США все заводы, введенные в эксплуатацию после 1972 г., оборудованы системами сухой очистки газов.
Мокрая очистка газа от фтористых соединений. Отходящий газ сразу (или после очистки его от пыли в электрофильтрах) подается в систему мокрой очистки для улавливания газообразных фторсодержащих и сернистых соединений. В качестве таких установок применяются пенные аппараты и скрубберы различных типов.
Для улавливания газообразных фторидов используется раствор кальцинированной соды Na2CO3 с концентрацией 25— 50 г/л. Раствор готовят в отделении регенерации криолита и 1 подают на циркуляцию в скруббер. В процессе газоочистки протекают следующие реакции:
HF + Na2CO3 = NaF + NaHCO3;
NaHCO3 + HF = NaF + H2O + CO2;
Na2CO3 + 2HF = 2NaF + H2O + CO2;
Na2CO3 + SO2 + 0,5O2 = Na2SO4 + CO2;
Na2CO3 + CO2 + H2O = 2NaHCO3.
При достижении концентрации фторида натрия NaF в растворе 15—25 г/л его откачивают в отделение регенерации для варки криолита.
Скрубберы представляют собой цилиндрические или прямоугольные вертикальные башни, внутри которых проходит газ, а в его поток вводится раствор. В «скрубберах с насадкой, предназначенной для образования большей поверхности со- х прикосновения раствора и очищаемого газа, газ вводится снизу и выходит сверху, а раствор подается сверху и выводится снизу. В полых скрубберах и газ, и раствор подают сверху и выводят снизу. В этом случае достигается более равномерное распределение газа по сечению скруббера.
Гидравлическое сопротивление скруббера составляет 1 кПа, рабочий диапазон скорости газа в скруббере 5—9 м/с, плотность орошения 35—50 м3/(м2-ч), расчетная эффективность очистки 99,6 %.
В алюминиевой промышленности применялись насадочные скрубберы с насадками из керамических колец Рашига диаметром и высотой 100 мм и толщиной стенки 10 мм, которые укладывались на поддерживающую решетку рядами. Как показал опыт их эксплуатации, очистка насадки от накапливающейся пыли и осадков очень сложна и трудоемка и при большом количестве аппаратов превращается в трудноразрешимую проблему. Такие скрубберы находят крайне ограниченное применение. Кроме того, их гидравлическое сопротивление в 2—4 раза выше, чем у полых скрубберов, которые в последние годы получили большое распространение. Безнасадочные (полые) скрубберы работают на скоростях газа 4—9 м/с, и в них нет газораспределительных устройств. Орошение скруббера ведется относительно крупными каплями раствора при плотности не менее 40—60 м3/(м2-ч) [2—3 м3/1000 м3 газа].
Мокрая газоочистка обладает высокой эффективностью улавливания газообразных примесей, но имеет ряд существенных недостатков: необходимость подготовки и оборота растворов, наличие шламовых полей, каплеунос, коррозия и эрозия аппаратуры и др. Возврат в процесс электролиза фторидов осуществляется путем их регенерации в гидрохимических процессах, которые осуществляются в специальных цехах. От этих недостатков свободны сухие системы очистки газов, широко используемые за рубежом и на некоторых заводах СНГ.
Сухая очистка отходящих газов основана на адсорбции HF глиноземом. Этот принцип является общим для всех аппаратурно-технологических схем сухой очистки анодных газов. Процесс очистки схематично может быть представлен следующим образом:
А12О3 + HF → Al2O3nHF → A1F3 + H2O (газ).
Адсорбционная способность глинозема, т.е. его способность улавливать на своей поверхности фтористый водород, зависит от содержания активной модификации глинозема (у-А12О3), способной его адсорбировать, и от его удельной поверхности. Выполненные ВАМИ исследования показали, что каждый грамм промышленного глинозема может адсорбировать 0,013 % HF, или 1,3 %, при этом степень улавливания фтористого водорода сохраняется на уровне 99— 99,5 % при времени контакта глинозема с газом в течение 1-3 с.
Все схемы сухой очистки газов состоят из:
- устройства для контактирования газа с глиноземом (реактор);
- пылеуловителя для улавливания глинозема и другой пыли;
- системы транспорта глинозема;
- дымососа для транспортировки газа;
- автоматизированной системы управления процессом.
Конечным продуктом при сухой очистке газов является фторированный глинозем, возвращаемый в электролизеры без какой-либо переработки. Таким образом, сухая газоочистка — практически безотходная технология.
Фторированный глинозем помимо HF содержит уловленную электролизную пыль, куда входят твердые фториды, углерод и др., которые, попадая в электролизер, снижают качество алюминия. Рост содержания примесей в глиноземе прямо пропорционален кратности циркуляции глинозема через реактор и количеству, используемому для сухой очистки. Минимальный прирост примесей имеет место при работе реактора без циркуляции, т.е. при использовании всего глинозема "на проток".
Наиболее широко внедрены в производство системы сухой очистки газов, разработанные компаниями "Flakt" и "Procedair". Несмотря на большое разнообразие конструктивных решений, наибольший интерес представляет устройство для контактирования отходящего газа с пылью (реактор) и устройство для улавливания фторированного глинозема.
На рис. 12.4, а приведена схема очистки газов с подачей глинозема в поток очищаемого газа через насадку Вентури, которая обеспечивает хорошее турбулентное перемешивание глинозема в потоке газов. Большинство таких реакторов оснащены устройствами для рециркуляции глинозема, что повышает эффективность улавливания HF, но вызывает дополнительную истираемость глинозема и увеличивает абразивный износ оборудования.
Другим типом реакторов (рис. 12.4, б) является система с кипящим слоем. В этой системе очищаемый газ контактирует с глиноземом путем пропускания поднимающегося потока газа через "кипящий" слой глинозема, который движется вдоль горизонтального перфорированного листа, а поток газа проходит через отверстия, создавая эффект кипящего слоя. Свежий глинозем подается с одной стороны реактора и удаляется с другого конца, а для улавливания унесенных потоком газа частиц глинозема используется рукавный фильтр.
Преимущество системы с кипящим слоем состоит в том, что при нарушении на несколько часов подачи глинозема кипящий слой сохраняет способность эффективно улавливать фториды. Кроме того, в таких системах весь глинозем про ходит через реактор, что упрощает систему его подачи. Основным недостатком этой системы является то, что кипящий слой создает большой перепад давлений и, следовательно, требует большого расхода электроэнергии.
В подавляющем большинстве систем в качестве пылеуловителей применяют рукавные фильтры, изготавливаемые из иглопробивного нетканого полиэфирного полотна, или электрофильтры.
Регенерация рукавных фильтров (очистка их от осевшего фторированного глинозема) осуществляется импульсной подачей воздуха низкого давления, что уменьшает износ рукавов и увеличивает срок их службы, который, по данным Саянского алюминиевого завода, составляет не менее 5 лет.
Все ведущие фирмы по производству газоочистных сооружений применяет модульный принцип. Модуль состоит из реактора и рукавного фильтра и способен очистить от 70 до 100 тыс. м3/ч. Из таких модулей собирается установка, к которой может быть подключена определенная группа ванн.