КРИСТАЛЛИЗАЦИЯ СТАЛИ
Образование зародыша и рост кристалла
Сущность процесса кристаллизации стали заключается в переходе ее из жидкого состояния в твердое.
При понижении температуры увеличивается вероятность существования образований (кристаллов или роев) с упорядоченным строением, а их структура приближается к структуре твердого кристалла. При определенной температуре, называемой температурой кристаллизации, термодинамически одинаково вероятно наличие в системе как жидкой, так и твердой фаз. При этой температуре свободная энергия чистого металла в жидком и твердом состояниях одинакова.
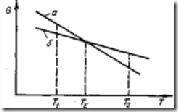
Изменение свободной энергии G чистого металла в жидком (а) и твердом (б) состояниях в зависимости от температуры Т
Из схемы следует, что выше температуры кристаллизации (плавления) Т2 > Те устойчивым является жидкое состояние Gж < Gтв. При снижении температуры ниже Те термодинамически устойчива твердая фаза.
Таким образом, при температуре Те возможно возникновение кристаллика, который при определенных условиях может расти, питаясь из окружающей жидкой фазы.
При охлаждении жидкости до температуры плавления кристаллизация начинается не сразу. Возникающие в жидкости кристаллические образования непрочны и легко разрушаются. Для образования устойчивых первичных кристаллов необходимо переохлаждение, т. е. некоторое снижение температуры ниже точки плавления.
Сталь в изложницах кристаллизуется или затвердевает в виде кристаллов древовидной формы — дендритов. Процесс кристаллизации складывается из двух стадий — зарождения кристаллов и последующего их роста. Различают гомогенное и гетерогенное зарождение кристаллов.
Под гомогенным подразумевают образование зародышей кристалла в объеме жидкой фазы, под гетерогенным — на имеющейся межфазной поверхности (на поверхности находящихся в расплаве твердых частиц — например, неметаллических включений, стенок изложниц н кристаллизаторов).
Гомогенное зарождение - происходит следующим образом: в жидком металле вблизи точки кристаллизации вследствие флуктуации энергии, состава и плотности непрерывно образуются группировки атомов с упорядоченной структурой — комплексы или зародыши твердой фазы. Одновременно и непрерывно происходит разрушение большей части их них. С тем, чтобы зародыш стал термодинамически устойчивым, т. е. способным к дальнейшему росту необходимы определенные условия.
Условия гомогенного зарождения.
Из термодинамики известно, что переход жидкости в твердое состояние и наоборот возможны, если свободная энергия системы при этом уменьшается.
Затвердевание или расплавление в процессе изменения температуры объясняются тем, что при температурах, превышающих точку кристаллизации, меньшей удельной свободной энергией обладает жидкая фаза, а при более низких температурах — твердая.
В процессе образования зародыша свободная энергия системы с одной стороны возрастает в результате затраты энергии на образование поверхности раздела «расплав — зародыш»
![]()
и с другой стороны уменьшается в результате перехода части жидкости в твердую фазу, у которой уровень свободной энергии ниже
![]()
где σ – межфазное натяжение на границе раздела фаз (удельная поверхностная энергия).
При температуре кристаллизации свободная энергия жидкой и твердой фаз равны и образование зародыша невозможно, так как нет источника для компенсации затрат энергии на образование поверхности раздела фаз. Поэтому для образования зародыша необходимо некоторое переохлаждение раплава: чем больше переохлаждение, тем больше будет выигрыш свободной энергии при переходе из жидкого состояния в твердое.
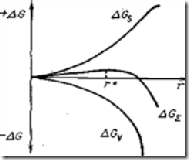 При данной величине переохлаждения термодинамически устойчивыми, т. е. способными к дальнейшему росту, оказываются те зародыши, размер которых превысит так называемый «критический». Критический размер это такой, начиная с которого дальнейший рост сопровождается снижением суммарной свободной энергии образования зародыша (рис).
При данной величине переохлаждения термодинамически устойчивыми, т. е. способными к дальнейшему росту, оказываются те зародыши, размер которых превысит так называемый «критический». Критический размер это такой, начиная с которого дальнейший рост сопровождается снижением суммарной свободной энергии образования зародыша (рис).
Величину критического радиуса зародыша определяют из соотношения:
![]()
где σ – межфазное натяжение на границе раздела жидкой и твердой фаз;
Ткр — температура начала кристаллизации;
ΔТ — величина переохлаждения;
QKp — скрытая теплота кристаллизации.
Таким образом, на процесс кристаллизации решающее влияние оказывают значения переохлаждения и удельной поверхностной энергии на границе кристалл—жидкость. При увеличении степени переохлаждения критический радиус зародыша уменьшается, т. е. термодинамически устойчивыми становятся более мелкие зародыши. То есть, чем выше степень переохлаждения, тем выше будет интенсивность образования устойчивых зародышей. Аналогичное влияние оказывает уменьшение величины поверхностной энергии σ.
Приближенные расчеты показывают, что гомогенное зарождение кристалла ряда металлов возможно при переохлаждении, равном 0,2•Ткр, т. е. около 350 °С для железа. Уменьшение переохлаждения до 200 °С снижает вероятность образования равновесного зародыша при гомогенной кристаллизации почти в 105 раз. Однако величина переохлаждения в стальном слитке обычно не превышает 10 °С. Следовательно, кристаллизация по гомогенному механизму на практике не реализуется.
В реальных условиях механизм затвердевания имеет гетерогенный характер, когда образование и рост зародыша происходят на уже имеющейся поверхности раздела – центрах кристаллизации (неметаллические включения или уже образовавшиеся в объеме кристаллы, стенки изложницы или формы, поверхность затвердевшей части слитка и т. п). Процесс зарождения и роста кристаллов в этом случае существенно облегчается - в реальных условиях сталь начинает кристаллизоваться при переохлаждении в несколько градусов. Следовательно, в реальных условиях происходит преимущественно гетерогенное зарождение кристаллов.
Введением центров кристаллизации широко пользуются на практике для модифицирования (улучшения) структуры слитка или отливки. При этом измельчается зерно и повышаются свойства металла. В качестве модифицирующих добавок служат обычно тугоплавкие оксиды, нитриды, имеющие температуры плавления выше, чем стали, и образующиеся в стали при введении таких активных элементов, как РЗМ, Ti, Zr и т. п.
Эффект модифицирования может иметь место также при введении в расплав поверхностно-активной добавки, снижающей величину межфазного натяжения на границе жидкость—твердая фаза. При этом уменьшается энергетический барьер образования новой границы раздела фаз и облегчается зарождение новых кристаллов, а следовательно, измельчается структура металла.
В формировании структуры слитка не меньшую роль играет последующий рост кристаллов, который обусловливается прежде всего интенсивностью и направленностью отвода тепла.


